
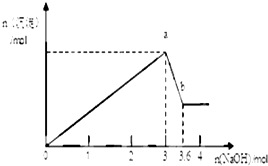
 有一无色透明溶液,可能含Al3+、Fe3+、Mg2+、Na+、CO
有一无色透明溶液,可能含Al3+、Fe3+、Mg2+、Na+、CO2- 3 |
- 3 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:0103 期中题 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:
(9分)某固体混合物可能由KCl、K2SO4、KI、NaNO3、CuCl2、CaCl2和Na2CO3中的一种或几种混合而成,为鉴定其组成依次进行如下实验:
①混合物中加入足量水得一无色透明溶液
②上述溶液中滴加BaCl2溶液有白色沉淀产生,将沉淀滤出并将滤液分成两份
③上述白色沉淀加盐酸时,沉淀部分溶解
④向一份滤液中加氯水及CCl4振荡静置,CCl4层显紫色
⑤往另一份滤液中加AgNO3溶液有白色沉淀产生,该沉淀不溶于稀HNO3
根据以上实验可判断:
⑴肯定存在的物质有_________________________________
肯定不存在的物质有 ____________________
⑵写出步骤③④中有关反应的离子方程式:
____________________________________________、
____________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com