
某学生对SO2与漂粉精的反应进行实验探究:
| 操 作 | 现 象 |
| 取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
|
| ⅰ.液面上方出现白雾; ⅱ.稍后,出现浑浊,溶液变为黄绿色; ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是___________________________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是________。
(3)向水中持续通入SO2,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
①实验a的目的是________。
②由实验a、b不能判断白雾中含有HCl,理由是____________________________。
(4)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。通过进一步实验确认了这种可能性,其实验方案是________。
(5)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是________。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因:_____________________________。
答案 (1)2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
(2)碱性、漂白性
(3)①检验白雾中是否含有Cl2,排除Cl2干扰
②白雾中混有SO2,SO2可与酸化的AgNO3反应产生白色沉淀
(4)向漂粉精溶液中逐滴加入稀硫酸,观察溶液是否变为黄绿色
(5)①CaSO4
②SO2+Cl2+2H2O===SO +2Cl-+4H+
+2Cl-+4H+
解析 (1)联系氯的化合物基础知识和生产漂粉精的原理,其化学方程式:2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O。
(2)pH试纸先变蓝,说明漂粉精溶液呈碱性,后褪色是由于ClO-的强氧化性所致。
(3)检验白雾中有无HCl的关键是检验出Cl-的存在,故实验a、b即围绕Cl-的检验展开。实验a的目的是通过湿润碘化钾淀粉试纸是否变蓝判断有无Cl2的干扰。实验b试图通过AgCl的生成来检验Cl-的存在,但应考虑到过量SO2和AgNO3溶液反应生成白色沉淀。
(4)题干具有明显的提示性,出现黄绿色的原因是随着酸性的增强而产生Cl2。故应设计使用无还原性的稀硫酸来确认其可能性。
(5)①A瓶中所得沉淀的成分可能是CaSO3、CaSO4或二者的混合物,加入稀HCl,无明显变化,排除CaSO3,故X为CaSO4,因CaSO4微溶于水,再取上层清液加入BaCl2溶液时,产生BaSO4沉淀,进一步证明X为CaSO4。
②溶液呈黄绿色是因Cl2溶于水而产生的现象,随着SO2的持续通入,两者发生反应生成无色物质盐酸和硫酸,化学方程式为SO2+Cl2+2H2O===2HCl+H2SO4,离子方程式为SO2+Cl2+2H2O===4H++SO +2Cl-。
+2Cl-。


科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)原子的最外层有2个电子的元素一定是ⅡA族元素( )
(2)元素所在的主族序数与最外层电子数之比为1的元素都是金属元素( )
(3)原子及离子的核外电子层数等于该元素所在的周期数( )
(4)原子最外层电子数大于3(小于8)的元素一定是非金属元素( )
(5)某元素的离子的最外层与次外层电子数相同,该元素一定位于第3周期( )
(6)最外层电子数等于或大于3(小于8)的一定是主族元素( )
(7)最外层有1个或2个电子,则可能是ⅠA、ⅡA族元素,也可能是副族、Ⅷ族元素或0族元素氦( )
(8)最外层电子数比次外层电子数多的元素一定位于第2周期( )
(9)某元素阴离子最外层电子数与次外层相同,该元素位于第3周期;若为阳离子,则位于第4周期( )
(10)电子层结构相同的离子,若电性相同,则位于同周期,若电性不同,则阳离子位于阴离子的下一周期——“阴上阳下”规律( )
查看答案和解析>>
科目:高中化学 来源: 题型:
油脂既是重要的食物,又是重要的化工原料。油脂的以下性质和用途与其含有的不饱和碳碳双键有关的是( )
A.适量摄入油脂,有助于人体吸收多种脂溶性维生素和胡萝卜素
B.利用油脂在碱性条件下水解,可以生产甘油和肥皂
C.植物油通过氢化,即与氢气发生加成反应,可以制造植物奶油(人造奶油)
D.油脂没有固定的熔、沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是某蛋白质的结构片段:
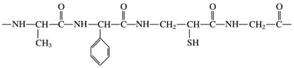
(1)上述蛋白质结构片段的水解产物中不属于α氨基酸的结构简式为________________________________________________________________________。
(2)上述蛋白质结构片段水解后的氨基酸中,某氨基酸碳氢原子数比值最大。
①该氨基酸与NaOH溶液反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
②该氨基酸两分子缩合形成环状结构物质的分子式为
________________________________________________________________________
________________________________________________________________________。
③该氨基酸的同分异构体中,属于硝基化合物且苯环上只有甲基的同分异构体有________种。
(3)已知上述蛋白质结构片段的相对分子质量为364,则水解生成的各种氨基酸的相对分子质量之和为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知亚硫酸钠在空气中能被氧气氧化生成硫酸盐。
Ⅰ.甲同学设计两种方案来检验Na2SO3溶液是否发生变质。
方案一:取样,加入稀盐酸有气泡生成,认为亚硫酸钠溶液没有变质。
方案二:取样,加入氯化钡溶液有白色沉淀生成,认为亚硫酸钠溶液完全变质。
请你对两方案作出评价:
方案一:________(填“合理”或“不合理”),理由是________________________________。
方案二:________(填“合理”或“不合理”),理由是___________________。
Ⅱ.乙同学探究Na2SO3溶液是否发生变质,设计如下实验测定1.0 mol·L-1 Na2SO3溶液的实际浓度。
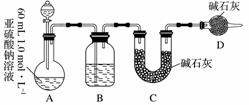
(1)分液漏斗中应加入足量的下列哪种试剂?________(填字母)
a.浓硝酸 b.65%硫酸 c.浓盐酸
(2)实验前后测得C装置增重3.2 g,则Na2SO3溶液实际的物质的量浓度为________。
(3)该实验装置还存在一个明显的缺陷是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语表示正确的是( )
①甲基的电子式: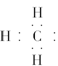
②乙炔的最简式:C2H2
③蔗糖的分子式:C12H22O11
④乙醛的结构简式:CH3COH
⑤苯分子的比例模型: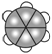
A.①②④ B.③⑤
C.②③⑤ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
从化学键的观点看,化学反应的实质是“旧键的断裂,新键的形成”,据此你认为下列变化属于化学变化的是 ( )
①对空气进行降温加压 ②金刚石变成石墨 ③NaCl熔化 ④碘溶于CCl4中 ⑤HCl溶于水电离出H+和Cl- ⑥电解熔融的Al2O3制取Al
A.②③⑤ B.②⑤⑥
C.②⑥ D.②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在密闭容器中SO2、O2、SO3三种气态物质建立化学平衡后,改变条件对反应2SO2(g)+O2(g)2SO3(g),ΔH<0的正、逆反应速率的影响如图所示:
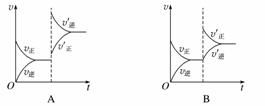
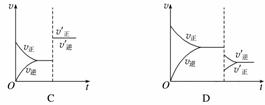
(1)加催化剂对反应速率影响的图像是________(填序号,下同),平衡________移动。
(2)升高温度对反应速率影响的图像是__________,平衡向________方向移动。
(3)增大反应容器体积对反应速率影响的图像是________,平衡向________方向移动。
(4)增大O2的浓度对反应速率影响的图像是__________,平衡向________方向移动。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com