

| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物安全沉淀 | 3.2 | 9.0 | 6.7 | |


科目:高中化学 来源:不详 题型:单选题
| A.BaCl2 | B.NaOH | C.Ba(OH)2 | D.AgNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.检验试液中的SO42-:试液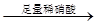 无沉淀 无沉淀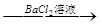 白色沉淀 白色沉淀 |
B.检验试液中的Fe2+:试液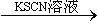 无明显现象 无明显现象 红色溶液 红色溶液 |
C.检验试液中的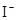 :试液 :试液 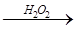 棕黄色溶液 棕黄色溶液 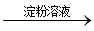 蓝色溶液 蓝色溶液 |
D.检验试液中的CO32-:试液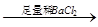 白色沉淀 白色沉淀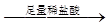 沉淀溶解 沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.萃取; | B.升华; | C.结晶; | D.分液;E.蒸馏;F.层析;G.过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
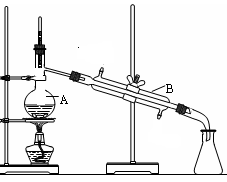
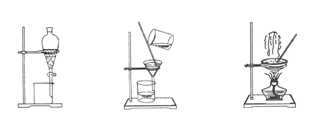
| A.烧杯 | B.坩埚 | C.表面皿 | D.泥三角 E.酒精灯 F.干燥器 |
查看答案和解析>>
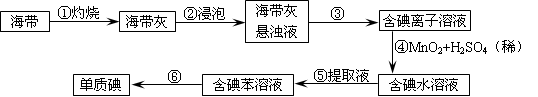
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 物质 | 选用试剂(过量) | 操作方法 |
| A | Cu(CuO) | 氧气 | 通入氧气并加热 |
| B | CO2(HCl) | 饱和碳酸氢纳溶液 | 通过盛有饱和碳酸氢纳溶液的洗气瓶 |
| C | CO(H2) | 氧化铜 | 通过灼热的氧化铜 |
| D | KCl溶液(K2CO3) | 氯化钙溶液 | 加入氯化钙溶液充分反应后过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | 操 作 步 骤 | 现 象 及 结 论 |
| 方法一 | | |
| 方法二 | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
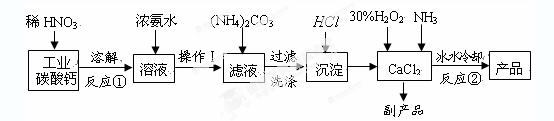
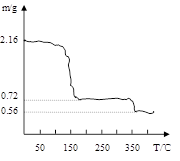
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com