
向某无色溶液中分别进行下列操作,所得现象和结论正确的是( )
A.加入氨水,产生白色沉淀,证明原溶液中存在Al3+
B.加入AgNO3溶液,产生白色沉淀,证明原溶液中存在Cl-
C.加入盐酸酸化的BaCl2溶液,生成白色沉淀,证明原溶液中存在SO
D.加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,证明原溶液中存在NH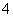
科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说法中正确的是
A.上述四种元素的原子半径大小为W<X<Y<Z
B. W与Y可形成既含极性共价键又含非极性共价键的化合物
C. W、X、Y、Z原子的核外最外层电子数的总和为20
D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
CO(g)+H2O(g)  H2(g)+CO2(g) ΔH<0,在其他条件不变的情况下
H2(g)+CO2(g) ΔH<0,在其他条件不变的情况下
A.加入催化剂,加快了反应速率,反应的ΔH也随之改变
B.温度降低,正、逆反应速率都减小,反应放出的热量不变
C.恒容时充入稀有气体或充入H2,正、逆反应速率都减小
D.改变压强,反应速率发生改变,反应放出的热量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制硫酸生产流程如下图:
|

(1)在沸腾炉中,需要将黄铁矿粉碎的目的是 。
(2)在催化反应室,下列措施中有利于提高SO2平衡转化率的有 。(填写编号)
a.减少压强 b.升高温度 c.不断补充空气 d.及时分离出SO3
(3)在生产中,为提高催化剂效率采取的措施有 , (答出2点)。
(4)在450℃、常压和钒催化条件下,在容积为VL的恒容容器中加入2n molSO2和n molO2
判断反应达到平衡状态的标志是 。(填写编号)
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
反应达若平衡后测得平衡常数为K,此时O2的转化率为x,则K和x的关系满足K= 。
(5)图1、2表示该SO2和O2的反应在时刻t1达到平衡、在时刻t2因改变某个条件而发生变化的情况:
① 图1中时刻t2发生改变的条件是 。
② 图2中时刻t2发生改变的条件是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验装置的说法中正确的是( )

A.用图1装置制取干燥纯净的NH3
B.用图2装置实验室制备Fe(OH)2
C.用图3装置可以完成“喷泉”实验
D.用图4装置测量Cu与浓硝酸反应产生气体的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液只可能含有以下离子中的若干种:H+、NH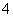 、K+、Mg2+、NO
、K+、Mg2+、NO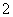 、CO
、CO 、NO
、NO ,现取两份200 mL溶液进行如下实验:(已知HNO2不稳定极易分解2HNO2===H2O+NO2↑+NO↑)
,现取两份200 mL溶液进行如下实验:(已知HNO2不稳定极易分解2HNO2===H2O+NO2↑+NO↑)
①第一份加足量AgNO3溶液后,有11.68 g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.2 g;②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀2.0 g,该沉淀能溶于稀盐酸产生无色气体;③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用100 mL 0.5 mol·L-1的稀硫酸恰好完全吸收,酸也不剩余。
根据上述实验,以下推测不正确的是( )
A.原溶液一定不存在较大浓度的H+、Mg2+
B.原溶液确定含NH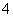 、NO
、NO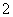 、CO
、CO ,且物质的量之比为5:2:1
,且物质的量之比为5:2:1
C.不能确定原溶液是否含有K+、NO
D.实验中产生的棕色气体遇空气颜色会加深
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质和用途的说法,正确的是( )
A.光导纤维具有很强的导电能力,所以大量用于制造通信光缆
B.明矾常用作净水剂,是因为它具有消毒杀菌的作用
C.氨常用作制冷剂,是因为其沸点极低,很容易液化
D.SiCl4在战争中常用作烟雾弹,是因为它与水反应时生成白色烟雾
查看答案和解析>>
科目:高中化学 来源: 题型:
卤素单质的性质活泼,卤素的化合物应用广泛,运用化学反应原理研究卤族元素的有关性质具有重要意义。
(1)下列关于氯水的叙述正确的是________(填写序号)。
A.氯水中存在两种电离平衡
B.向氯水中通入SO2,其漂白性增强
C.向氯水中通入氯气,c(H+)/c(ClO-)减小
D.加水稀释氯水,溶液中的所有离子浓度均减小
E.加水稀释氯水,水的电离平衡向正反应方向移动
F.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)工业上通过氯碱工业生产氯气,其反应的离子方程式为____。
(3)常温下,已知25 ℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | K=3.0×10-8 | K1=4.4×10-7,K2=4.7×10-11 |
写出84消毒液(主要成分为NaClO)露置在空气中发生反应的有关化学方程式________________________。若将84消毒液与洁厕剂(含有浓盐酸)混合使用可能会导致中毒,请用离子方程式解释有关原因__________________。
(4)碘钨灯具有比白炽灯寿命长且环保节能的特点。一定温度下,灯内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g)WI2(g)。为模拟上述反应,准确称取0.508 g碘、0.736 g金属钨置于50.0 mL的密闭容器中,加热使其反应。
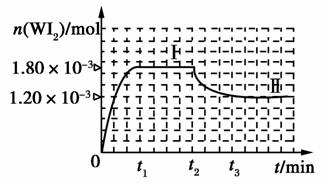
如图是WI2(g)的物质的量随时间变化的关系图像,其中曲线I(0~t2时间段)的反应温度为T1,曲线Ⅱ(从t2开始)的反应温度为T2,且T2>T1。则:
①该反应的ΔH________0(填“>”、“=”或“<”)。
②从反应开始到t1时间内的平均反应速率v(I2)=________。
③下列说法中不正确的是________(填序号)。
A.利用该反应原理可以提纯钨
B.该反应的平衡常数表达式是K=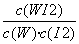
C.灯丝附近温度越高,灯丝附近区域WI2越易变为W而重新沉积到灯丝上
(5)25 ℃时,向5 mL含有KCl和KI浓度均为0.1 mol·L-1的混合液中,滴加6 mL 0.1 mol·L-1的AgNO3溶液,先生成的沉淀是________,溶液中离子浓度由大到小的顺序是________[不考虑H+和OH-。25 ℃时Ksp(AgCl)=1.8×10-10、Ksp(AgI)=8.3×10-17]。
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期主族元素A、B、C、D的原子序数依次增大,它们的原子序数之和为36,最外层电子数之和为14;A、C原子的最外层电子数之和等于B原子的次外层电子数,B、D同主族。下列叙述不正确的是
A.A、B、D三种元素形成的化合物一定是强酸
B.B元素在地壳中的含量一定最高
C.C元素在元素周期表中一定位于第三周期第ⅠA族
D.D元素与氢元素形成化合物的化合物常温下一定为气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com