
已知25℃时有关弱电解质的电离平衡常数如下表:
| 弱电解质化学式 | CH3COOH | HCN | H2CO3 | NH3.H2O |
| 电离平衡常数 | 1.8×l0–5 | 4.9×l0–10 | K1=4.3×l0–7 K2=5.6×l0–11 | 1.8×l0–5 |
根据上表中数据回答下列问题:
(1)CH3COO- 、CN- 、CO32-结合质子(即H+)的能力大小顺序_____________________;25℃时,有等浓度的①CH3COONa溶液、②NaCN溶液、③NaHCO3溶液,三种溶液的pH由大到小的顺序为 (填序号)。
(2)Na2CO3水溶液呈碱性的原因,用离子方程式表示: ,
溶液中各离子浓度大小顺序: 。
(3) NaCN溶液中通入少量二氧化碳,反应的离子方程式为
(4)室温下,向盛一定量的稀氨水烧杯中逐滴加入物质的量浓度相同的醋酸,当恰好中和时,溶液的pH 7(填“大于”、“等于”或“小于”)。
(5)甲、乙两瓶氨水的浓度分别为1mol·L-1、0.1mol·L-1,
则c(OH-)甲﹕c(OH-)乙 10(填“大于”、“等于”或“小于”)。
科目:高中化学 来源: 题型:
铜锌合金的颜色酷似金的颜色,所以近来用铜锌合金制成的假金元宝欺骗行人的事件屡有发生。要检验市面上的金首饰是否为纯金或者真金,可取样品与一种试剂进行反应,根据现象即可判断 ,所取的试剂不能是
A.硫酸 B.“王水” C.盐酸 D.硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法中不正确的是 ( )
A.甲烷与氯气在光照条件下的反应和乙酸与乙醇生成乙酸乙酯的反应均属于
取代反应
B.顺-2-丁烯和反-2-丁烯的熔、沸点不相同
C.C4H9Br的同分异构体有3种
D.乙烯、苯分子中的所有原子都在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是
A.NH3(g)+HCl(g)→NH4Cl(s),该反应可自发进行,故熵值增大
B.SO2(g) →S(s)+O2(g) △H>0,△S<0。则该反应能自发进行
C.O2(g)+2H2(g)= 2H2O(l) △H<0,恒温恒压下一定能自发进行
D.某温度下2SO2(g)+O2(g)  2SO3(g),K1=400,则相同温度下
2SO3(g),K1=400,则相同温度下
2SO3(g) 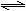 2SO2(g)+O2(g)的平衡常数为1/400
2SO2(g)+O2(g)的平衡常数为1/400
查看答案和解析>>
科目:高中化学 来源: 题型:
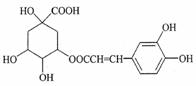 咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示。关于咖啡鞣酸的下列说法正确的是
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示。关于咖啡鞣酸的下列说法正确的是
A.分子式为C16H18O9
B.1mol咖啡鞣酸水解时可消耗8molNaOH
C.咖啡鞣酸分子中所有原子都在同一平面上
D.与浓溴水既能发生取代反应又能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
如图X、Y、A、B、C均为短周期主族元素,其中只有一种是金属元素,则下列说法错误是( )
| X | A | ||
| Y | C | B |
|
| A. | 原子半径大小:Y>C>X>A |
|
| B. | Y和B形成的化合物中Y和B的原子个数比为2:3 |
|
| C. | X、C、A中最高价氧化物对应的水化物的酸性最强的是A |
|
| D. | A、B均为非金属元素,所以两者的氢化物相遇不发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来大气问题受到人们越来越多的关注.按要求回答下列问题:
Ⅰ.实现反应CH4(g)+CO2(g)⇌2CO(g)+2H2(g),△H0,对减少温室气体排放和减缓燃料危机具有重要意义.在2L密闭容器中,通入5mol CH4与5mol CO2的混合气体,一定条件下发生上述反应,测得CH4的平衡转化率与温度、压强的关系如图1.
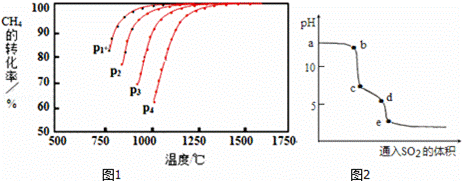
则p1、p2、p3、p4由大到小的顺序 P4>P3>P2>P1 ,该反应的正反应是 吸热 (填“吸热”或“放热”)反应,当1000℃甲烷的转化率为80%时,该反应的平衡常数K= 1024 .
Ⅱ.PM2.5污染与直接排放化石燃烧产生的烟气有关,化石燃料燃烧同时放出大量的SO2和NOx.
(1)处理NOx的一种方法是利用甲烷催化还原NOx.
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=﹣574kJ•mol﹣1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=﹣1160kJ•mol﹣1
CH4(g)+2NO2 (g)=N2(g)+CO2(g)+2H2O(g)△H3
则△H3= ﹣867kJ•mol﹣1 ,如果三个反应的平衡常数依次为K1、K2、K3,则K3= 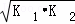 (用K1、K2表示)
(用K1、K2表示)
(2)实验室可用NaOH溶液吸收SO2,某小组同学在室温下,用pH传感器测定向20mL0.1mol•L﹣1NaOH溶液通入SO2过程中的pH变化曲线如图2所示.
①ab段发生反应的离子方程式为 SO2+2OH﹣=SO32﹣+H2O .
②已知d点时溶液中溶质为NaHSO3,此时溶液中离子浓度由大到小的顺序为 c(Na+)>c(HSO3﹣)>c(H+)>c(SO32﹣)>c(OH﹣) ,如果NaHSO3的水解平衡常数Kh=1×10﹣12mol•L﹣1,则该温度下H2SO3的第一步电离平衡常数Ka= 10﹣2mol•L﹣1 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com