
| A、υ(H2O)=0.45 mol?L-1?s-1 |
| B、υ(O2)=0.010 mol?L-1?s-1 |
| C、υ(NO)=0.010 mol?L-1?s-1 |
| D、υ(NH3)=0.10 mol?L-1?s-1 |
| ||
| △t |
| ||
| △t |
| ||
| 30s |
| 5 |
| 6 |
| 2 |
| 3 |
| 2 |
| 3 |


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 | Cl-OH | 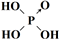 | 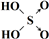 |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、推广和鼓励多使用公共交通工具出行 |
| B、大量使用化肥农药,提高农作物产量 |
| C、大力发展太阳能和风力发电 |
| D、对燃煤进行脱硫,减少空气的污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 1mol?L-1的Na2CO3 溶液中含有CO32-的数目为NA |
| B、常温常压下,22.4 L CH4中含有4 NA 个C-H键 |
| C、常温常压下,1.7gH2O2中含有的电子数为0.5 NA |
| D、1 mol Zn与足量稀HNO3反应,转移2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2可溶于水,新制氯水显浅黄绿色 |
| B、SO2能使品红溶液褪色说明SO2具有氧化性 |
| C、常温下,等体积的Cl2和SO2混合气体通入BaCl2溶液时,无明显现象 |
| D、等体积的Cl2和SO2分别通入含石蕊的水中,溶液的紫色立即褪去 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com