
室温下,下列叙述正确的是 ( )
A.pH=2的HA酸溶液与pH=12的MOH碱溶液以任意比混合:
c(H+) + c(M+)=c(OH-) + c(A-)
B.将物质的量浓度均为0.1mol·L−1的Na2CO3溶液、NaHCO3溶液等体积混合所得溶液中:2c(OH−)-2c(H+)=3c(H2CO3)+c(HCO3-)-c(CO32−)
C.等浓度、等体积的Na2CO3和NaHCO3混合: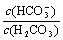 <
<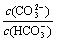
D.将足量AgCl分别放入:①5m水②10mL0.2mol/LMgC12③20mL0.3mol/L盐酸中溶解至饱和,c(Ag+):①>②>③
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
Ⅰ. 过氧化氢(H2O2)的水溶液俗称双氧水,近年来倍受人们的青睐,被称为“绿色氧化剂”。
(1)写出H2O2的电子式_________________
(2)你认为H2O2被称为“绿色氧化剂”的主要原因是______________________________
(3)将双氧水加入用盐酸酸化的FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式为_________________________________,反应中H2O2作_____________剂
(4)双氧水能使酸性高锰酸钾溶液褪色,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里:
MnO4-+___H2O2+_____H+ ===_____Mn2++____H2O+ 。
Ⅱ. 某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→ O2
⑴该反应的化学方程式为________________________________________________________
⑵如反应转移了0. 3mol电子,则产生的气体在标准状况下体积为
查看答案和解析>>
科目:高中化学 来源: 题型:
用20mL 18.4mol·L-1浓H2SO4与金属铜共热一段时间后,冷却,过滤,除去多余的铜,将滤液加水稀释到100mL,所得溶液中SO42-的物质的量浓度为3.18mol·L-1,则此时溶液中CuSO4的物质的量浓度为
A.0.05mol/L B.0.50 mol·L-1 C.0.75 mol·L-1 D.3.18 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
建构数学模型来研究化学问题,既直观又简洁。下列建构的数轴模型正确的是 ( )
A.钠在氧气中燃烧,钠的氧化产物: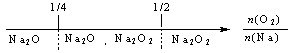
B.铁在Cl2中燃烧,铁的氧化产物: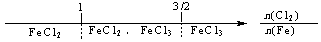 [来
[来
C.NH3与Cl2反应,反应产物: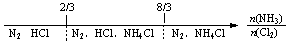
D.FeBr2溶液中通入Cl2,铁元素存在形式: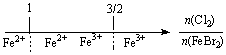
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸盐在能源、环保等方面有着广泛的用途。高铁酸钾(K2FeO4)易溶于水,具有强氧化性,是一种新型水处理剂。替代传统的净水剂及Cl2对淡水进行净化消毒是城市饮用水处理新技术。
工业上常用如下方法制备高铁酸钾:以铁丝网为阳极电解NaOH溶液,然后在阳极液中加入50%的KOH溶液,充分反应后,过滤、用异丙醇洗涤、干燥,即可制得。
(1)高铁酸钾具有强氧化性的原因是 ▲ 。
(2)用异丙醇代替水洗涤产品的好处是 ▲ 。
(3)高铁酸钾是一种理想的水处理剂,其处理水的原理为 ▲ , ▲ 。
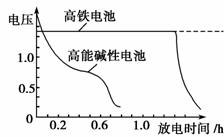
(4)高铁电池是正在研制中的可充电干电池,下图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有 ▲ 、 ▲ 。
(5)探究高铁酸钾的某种性质。
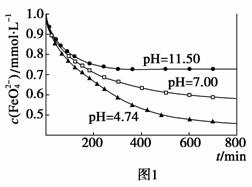 [实验1]将适量K2FeO4固体分别溶解于pH为4.74、7.00、11.50的水溶液中,配得FeO
[实验1]将适量K2FeO4固体分别溶解于pH为4.74、7.00、11.50的水溶液中,配得FeO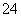 浓度为1.0 mmol·L-1(1 mmol·L-1=10-3 mol·L-1)的试样,静置,考察不同初始pH的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。
浓度为1.0 mmol·L-1(1 mmol·L-1=10-3 mol·L-1)的试样,静置,考察不同初始pH的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。
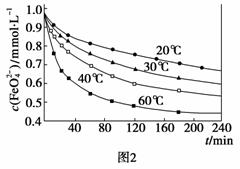
[实验2]将适量K2FeO4溶解于pH=4.74的水溶液中,配制成FeO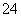 浓度为1.0 mmol·L-1的试样,将试样分别置于20 ℃、30 ℃、40 ℃和60 ℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则
浓度为1.0 mmol·L-1的试样,将试样分别置于20 ℃、30 ℃、40 ℃和60 ℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则
①实验1的目的是 ▲ ;
②实验2可得出的结论是 ▲ ;
③高铁酸钾在水中的反应为4FeO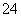 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑。
4Fe(OH)3+8OH-+3O2↑。
由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据有机物的命名原则,下列命名正确的是( )
|
| A. |
|
|
| B. | CH3CH(C2H5)CH2CH2CH3 2﹣乙基戊烷 |
|
| C. | CH3CH(NH2)CH2COOH α﹣氨基丁酸 |
|
| D. | 3,3﹣二甲基﹣2﹣丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:将一定量Cl2通入KOH溶液,可能生成KCl、KClO、KClO3,且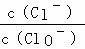 的值与温度高低有关.当n(KOH)=6a mol时,下列有关说法错误的是( )
的值与温度高低有关.当n(KOH)=6a mol时,下列有关说法错误的是( )
|
| A. | 若某温度下,反应后 |
|
| B. | 参加反应的氯气的物质的量等于3a mol |
|
| C. | 改变温度,反应中转移电子的物质的量ne的范围:3a mol<ne<5a mol |
|
| D. | 改变温度,产物中KClO3的最大理论产量为a mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
CO、H2在一定条件下合成乙醇:2CO(g)+4H2(g)  CH3CH2OH(g)+H2O(g)是一个放热反应。下列说
CH3CH2OH(g)+H2O(g)是一个放热反应。下列说
法错误的是( )
A.反应物的总能量大于生成物的总能量
B.增大H2浓度可以使CO转化率达到100%
C.使用合适的催化剂、升高温度均可加大反应速率
D.反应达到平衡时,正反应和逆反应的化学反应速率相等且不为零
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com