
海带中含碘元素,有人设计如下步骤来提取碘:①加入6%H2O2溶液 ②将海带烧成
灰,向灰中加入蒸馏水 ③加入CCl4振荡 ④过滤 ⑤用分液漏斗分液 ⑥加热煮沸
1~2分钟,合理的操作顺序为( )
A.②一⑥一④一①一③一⑤ B.②一①一⑥一③一④一⑤
C.②一①一③一⑥一⑤一④ D.②一③一①一⑥一⑤一④
科目:高中化学 来源: 题型:
氰气的化学式为(CN)2,结构式为N≡C—C≡N,性质与卤素相似,下列叙述正确的是
A.在一定条件下可发生加成反应
B.分子中N≡C键的键长大于C—C键的键长
C.分子中含有2个σ键和4个π键
D.不和氢氧化钠溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是( )
A.36gH2O和22.4LCO2中Si和O,C和O之间的共价键均是4×6.02×1023
B.0.1 L 3 mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023
C.常温常压下,4.6 g NO2气体含有0.1×6.02×1023个NO2分子
D.0.1 mol的甲基(—CH3)和羟基(—OH)所含电子数均为0.9×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
合成尿素的反应是分作两步进行的:
① 2CO2(g)+ NH3(g) H2NCOONH4(aq)(氨基甲酸铵) △H =-159.47kJ/mol
H2NCOONH4(aq)(氨基甲酸铵) △H =-159.47kJ/mol
②H2NCOONH4(aq) CO(NH2)2(aq)+ H2O(l) △H =-28.49kJ/mol
CO(NH2)2(aq)+ H2O(l) △H =-28.49kJ/mol
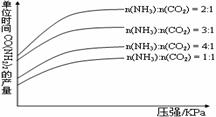
在生产条件下,单位时间内获得尿素的产量与压强和n(NH3):n(CO2)的关系如右图所示。生产过程中n(NH3):n(CO2)的最佳配比为 ,而实际实际生产条件下,往往使n(NH3):n(CO2)≥3,这是因为 。在得到的尿素溶液中会含有少量的氨基甲酸铵,除去这种杂质最简便的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用于判断元素金属性强弱的是( )
A.1 mol金属单质在反应中失去电子的多少
B.金属单质之间发生的置换反应
C.金属元素最高价氧化物对应的水化物的碱性强弱
D.金属元素的单质与水或酸置换出氢气的难易程度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质相互混合反应,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液 ②过量NaOH溶液和明矾溶液
③Ba(HCO3)2溶液和NaHSO4溶液 ④Na2O2投入FeCl3溶液
A.①④ B.②③④ C.②③ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
铝热反应常用于冶炼高熔点的金属, 可简单认为是铝与某些金属氧化物在高温条件下发生的反应。某学习小组对铝热反应(以Al和Fe2O3反应为例)实验进行研究。
查阅数据得到Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下表所示:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1565 |
| 沸点/℃ | 2467 | 2980 | 2750 | ┄ |
试回答下列问题:
(1)在铝热反应中金属铝表现出 性(填“氧化”或“还原”)。请判断下列金属中那一个不能由铝热反应制取 。(填序号)
①Fe ②Cr(铬) ③V(钒) ④Ca ⑤Mn
(2)某同学推测,铝热反应所得到的熔融物中应含有铁、铝两种金属。如设计一个简单的实验方案证明该熔融物中含有金属铝,则实验所需用的试剂为 ,可观察到的实验现象是 。
(3)另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物投入到少量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色未变血红色,即可证明熔融物中不含有Fe2O3。则
①物质甲是 (填化学式)。
②该同学的实验方案是否合理? (填“合理”或“不合理”)。
理由:
查看答案和解析>>
科目:高中化学 来源: 题型:
为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。

请回答:
(1)写出步骤Ⅰ反应的离子方程式: ▲ 。
(2)试剂X是 ▲ 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 ▲ 。
 (3)进行步骤Ⅱ时,该小组用如图7所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 ▲ 。
(3)进行步骤Ⅱ时,该小组用如图7所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 ▲ 。
(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式 ▲ ,请选出你认为的最佳途径并说明选择的理由 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的。在有关上述工艺流程的以下化学用语中,正确的是
A.用电子式表示溴化氢的形成过程为:
B.海水中Br-的电子式为:
C.海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl
D.氯离子的结构示意图为:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com