
(11分)下图为某实验者设计的验证银圆(银和铜的合金)完全溶解于一定量的浓硝酸后生成NO2气体中含有NO的实验装置图。常温时,NO2与N2O4同时存在;在低于0℃时,几乎只有无色的N2O4的晶体存在。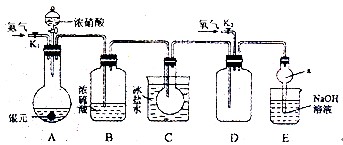
(1)反应前先打开A中的活塞K1,持续通一段时间N2,其理由是 。
(2)若装置中缺B,其后果是 。
(3)反应结束后,打开D中的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是 。
(4)C装置的作用是 ;E中a仪器所起的作用是 。
(5)已知该银圆的质量为25g,加入75mL 12mol·L—1的浓硝酸。实验结束后,A中烧瓶内溶液中H+的浓度为2mol·L—1(反应中HNO3既无挥发也无分解),溶液体积仍为75mL。
①参加反应的硝酸的物质的量是 。
②为测定该银圆中铜的质量分数,还需进行的主要实验操作是 。
(11分)(1)赶走装置中的空气,防止干扰实验。(1分)
(2)无法确认铜与硝酸反应是否生成了NO气体(1分)
(3)热的空气使平衡 2NO2  N2O4向逆方向移动,导致颜色加深(2分)
N2O4向逆方向移动,导致颜色加深(2分)
(4)将NO2 和NO分开(或除去二氧化氮气体) (2分) 防倒吸(1分)
(5) 0、75mol (2分) 向反应后的溶液中加入足量的盐酸,过滤洗涤称量干燥沉淀的质量 (2分)
以上各题合理的答案也可以。
解析试题分析:(1)由于装置中含有空气,而空气能把NO氧化生成NO2,从而干扰实验的检验,所以这样操作的目的是赶走装置中的空气,防止干扰实验。
(2)由于生成的气体中含有水蒸气,而NO2能和水反应生成NO,从而无法确认铜与硝酸反应是否生成了NO气体,所以不能缺少B装置。
(3)由于存在可逆反应2NO2 N2O4,该反应是放热反应,所以热的空气使平衡 2NO2
N2O4,该反应是放热反应,所以热的空气使平衡 2NO2 N2O4向逆方向移动,NO2浓度增大,从而导致颜色加深。
N2O4向逆方向移动,NO2浓度增大,从而导致颜色加深。
(4)由于在低于0℃时,几乎只有无色的N2O4的晶体存在,所以C装置的目的是通过降温将NO2 和NO分开(或除去二氧化氮气体)。由于NO2极易被氢氧化钠溶液吸收,如果直接插入会导致溶液的倒流,所以E中a仪器所起的作用是防倒吸。
(5)①硝酸的总的物质的量是0.9mol,剩余硝酸是0.15mol,所以参加反应的硝酸是0.9mol-0.15mol=0.75mol。
②由于反应后金属生成了硝酸盐,所以要测定该银圆中铜的质量分数,还需要把金属阳离子变成沉淀,然后通过称量即可计算,所以正确的操作可以是向反应后的溶液中加入足量的盐酸,过滤洗涤称量干燥沉淀的质量。
考点:考查物质的分离、外界条件对平衡的影响以及有关计算等
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。纵观近几年高考,主要以考察探究性实验和物质制备实验为主。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,要求考生必须冷静的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能正确作答。
探究性实验的一般思路
1、准确地把握实验目的
2、利用已学知识,分析如何实现这个目的--实验原理
3、结合实验材料,初步确定设计对策--实验方案


科目:高中化学 来源: 题型:
下图为某实验者设计的验证银圆完全溶解于一定量的浓硝酸,生成的NO2气体中含有NO的实验装置图。
常温时,NO2与N2O4混合存在;在低于0 ℃时,几乎只有无色N2O4晶体存在。
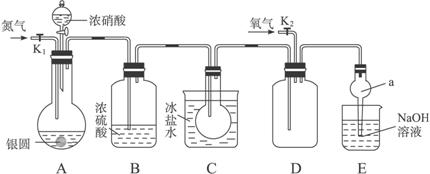
(1)反应前先打开A部分的活塞K1,持续通一段时间N2,其理由是_______________________
_____________________________________________________________________。
(2)若装置中缺B部分,其后果是_________________________________________________。
(3)反应结束后,打开D部分的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是_____________________________
_____________________________________________________________________。
(4)E部分中a仪器所起的作用是_________________________________________________。
(5)已知该银圆的质量为25 g,加入75 mL 12 mol·L-1的浓硝酸。实验结束后,A部分烧瓶内溶液中H+的浓度为2 mol·L-1(反应中HNO3既无挥发也无分解),体积仍为75 mL。
①参加反应的硝酸的物质的量为_________________________。
②为测定该银圆中铜的质量分数,还须进行的主要实验操作是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为某实验者设计的验证银圆完全溶解于一定量的浓硝酸后生成NO2气体中含有NO的实验装置图。常温时,NO2与N2O4同时存在;在低于0 ℃时,几乎只有无色的N2O4晶体存在。
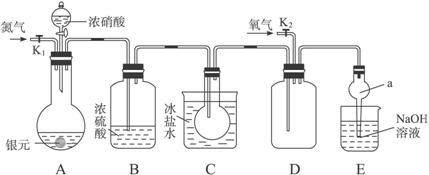
(1)反应前先打开A中的活塞K1,持续通一段时间N2,其理由是______________________。
(2)若装置中缺B,其后果是____________________________________________________。
(3)反应结束后,打开D中的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是____________________________。
(4)C装置的作用是______________________;E中a仪器所起的作用是________________。
(5)已知该银圆的质量为25 g,加入75 mL 12 mol·L-1的浓硝酸。实验结束后,A中烧瓶内溶液中H+的浓度为2 mol·L-1(反应中HNO3既无挥发也无分解),溶液体积仍为75 mL。
①参加反应的硝酸的物质的量是_________________。
②为测定该银圆中铜的质量分数,还需进行的主要实验操作是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)反应前先打开A中的活塞K1,持续通一段时间N2,其理由是___________________。
(2)若装置中缺B,其后果是_______________________。
(3)反应结束后,打开D中的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色,反应的化学方程式为________________________;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是____________________________________。(用方程式和必要的文字说明)
(4)C装置的作用是_______________________________________________________;
E中a仪器所起的作用是___________________________________________________。
(5)为测定该银圆中银的质量分数,还需进行的主要实验操作是:将A中溶液倒入烧杯中,然后加入过量的NaCl溶液,随后进行的操作为____________(用ABCD字母排序),最后测定溶液中Ag+的质量。
A.洗涤 B.过滤 C.称量 D.烘干
查看答案和解析>>
科目:高中化学 来源:2013届浙江省杭州市建人高复学校高三第二次月考化学试卷(带解析) 题型:实验题
(14分)下图为某实验者设计的验证银圆(银和铜的合金)完全溶解于一定量的浓硝酸后生成NO2气体中含有NO的实验装置图。常温时,NO2与N2O4同时存在;在低于0℃时,几乎只有无色的N2O4的晶体存在。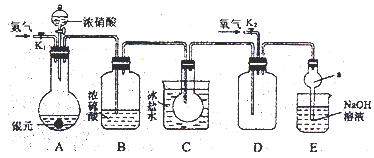
(1)反应前先打开A中的活塞K1,持续通一段时间N2,其理由是 。
(2)若装置中缺B,其后果是 。
(3)反应结束后,打开D中的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是 。
(4)C装置的作用是 ;E中a仪器所起的作用是 。
(5)已知该银圆的质量为25g,加入75mL 12mol·L—1的浓硝酸。实验结束后,A中烧瓶内溶液中H+的浓度为2mol·L—1(反应中HNO3既无挥发也无分解),溶液体积仍为75mL。
①参加反应的硝酸的物质的量是 。
②为测定该银圆中铜的质量分数,还需进行的主要实验操作是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com