
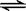 Na2S(s) + 4H2O(g) ��
Na2S(s) + 4H2O(g) �� ��2�����¶��£���2Lʢ��1.42 g Na2SO4���ܱ�������ͨ��H2���壬5���Ӻ��ù�������Ϊ1.10 g����5������H2��ƽ����Ӧ����Ϊ_________________��
��2�����¶��£���2Lʢ��1.42 g Na2SO4���ܱ�������ͨ��H2���壬5���Ӻ��ù�������Ϊ1.10 g����5������H2��ƽ����Ӧ����Ϊ_________________��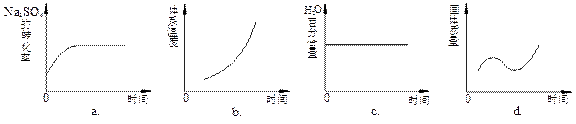

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Q(g) ��H��0��Ӱ�졣�����й�˵����ȷ����
2Q(g) ��H��0��Ӱ�졣�����й�˵����ȷ����
| A��x��������M��N��������� |
| B��x�����ǻ����������ʵ��� |
| C���÷�Ӧ��p1ʱ�ȴﵽ��ѧƽ��״̬ |
| D��p 1��p2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 xC��g��������ͼ��a������b����ʾ�Ĺ�ϵ���ߣ����ж����ж�ͼ��b����˵����ȷ���� �� ��
xC��g��������ͼ��a������b����ʾ�Ĺ�ϵ���ߣ����ж����ж�ͼ��b����˵����ȷ���� �� ��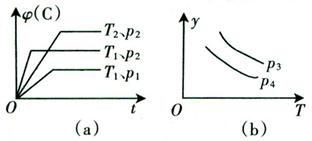
| A��p3��p4��y���ʾA��ת���� |
| B��p3��p4��y���ʾB��ת���� |
| C��p3��p4��y���ʾ���������ܶ� |
| D��p3��p4��y���ʾ���������A��Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 2NO��g��+O2��g������1molNO2��0.2molO2��һ������NOͨ���ݻ�Ϊ2L���ܱ������ڷ�Ӧ��10min��Ӧǡ�ôﵽƽ��״̬����ʱ��������0.6molNO��������ѹǿΪԭ����8/7�����㣺(Ҫ���м������)
2NO��g��+O2��g������1molNO2��0.2molO2��һ������NOͨ���ݻ�Ϊ2L���ܱ������ڷ�Ӧ��10min��Ӧǡ�ôﵽƽ��״̬����ʱ��������0.6molNO��������ѹǿΪԭ����8/7�����㣺(Ҫ���м������)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)��2 sʱ���C��Ũ��Ϊ0.6mol��L��1������˵����ȷ����
2C(g)��2 sʱ���C��Ũ��Ϊ0.6mol��L��1������˵����ȷ����| A��������A��ʾ��ƽ����Ӧ����Ϊ0.3mol/(L��s) |
| B��������B��ʾ��ƽ����Ӧ����Ϊ0.6mol/(L��s)�� |
| C��2 sʱ����A��ת����Ϊ70% |
| D��2 sʱ����B��Ũ��Ϊ0.7mol��L��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 qZ(g) ��H��0��m + n��q�������һ�����ܱ������дﵽƽ�⣬����������ȷ����( )
qZ(g) ��H��0��m + n��q�������һ�����ܱ������дﵽƽ�⣬����������ȷ����( )| A����Ӧ���ʦ���(X) =(n/m)����(Y) | B������X����Ӧ�ġ�H���� |
| C������Y�����ʵ�����X��ת�������� | D�������¶ȣ�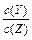 ��ֵ��С ��ֵ��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
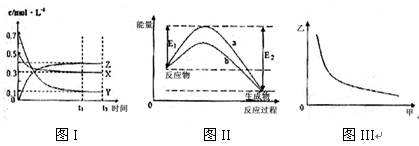

| A���÷�Ӧ�Ȼ�ѧ����ʽΪX(g) +3Y(g) 2Z(g)��H=�D��E2�DE1�� |
| B����ͼIII�мױ�ʾѹǿ���ұ�ʾZ�ĺ���������仯����ͼIII������ |
| C�����¶��£���Ӧ��ƽ�ⳣ����ֵԼΪ533���������¶ȣ��÷�Ӧ��ƽ�ⳣ����С��Y��ת���ʽ��� |
| D��ͼII������b�Ǽ������ʱ�������仯���ߣ�����a��û�м������ʱ�������仯���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com