
【题目】新装修的房屋会释放出有毒的甲醛气体。银-Ferrozine法检测甲醛(HCHO)的原理如下(在原电池中完成氧化银与甲醛的反应)。下列说法正确的是
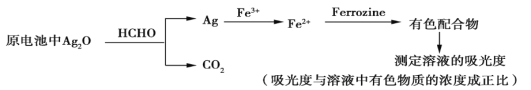
A. 其他条件相同,甲醛浓度越小,所得有色配合物溶液的吸光度越大
B. 电池正极的电极反应式为Ag2O+2H++2e-![]() 2Ag+H2O
2Ag+H2O
C. 30 g HCHO被氧化时,理论上电路中通过2 mol电子
D. 理论上,消耗HCHO和消耗Fe3+的物质的量之比为4∶1
【答案】B
【解析】
本题主要考查原电池的相关应用。HCHO中C为0价。该检测过程中设计的化学反应为2Ag2O+HCHO===4Ag+CO2+H2O,Ag+Fe3+===Ag++Fe2+,Fe2+与Ferrozine形成有色配合物。
A.吸光度与有色物质的浓度成正比,根据反应式可推出吸光度与甲醛的浓度成正比,错误;B.负极的电极反应式为:HCHO-4e-+H2O===CO2+4H+,正极的电极反应式为2Ag2O+4e-+4H+===4Ag+2H2O,正确;C.![]() ,负极消耗1mol HCHO理论上电路中通过4mol电子,错误;D.HCHO
,负极消耗1mol HCHO理论上电路中通过4mol电子,错误;D.HCHO![]() 4Ag
4Ag![]() 4Fe2+,1molCHO完全反应,理论上能生成4molAg消耗4molFe3+,错误。
4Fe2+,1molCHO完全反应,理论上能生成4molAg消耗4molFe3+,错误。


科目:高中化学 来源: 题型:
【题目】在2 L容器中有3种物质进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡。

(1)该反应的化学方程式是____________。
(2)反应起始至t时刻,Y的平均反应速率是_______________。
(3)关于该反应的说法,正确的是______。
A.到达t时刻该反应已停止
B.加入催化剂,一定能加快反应速率
C.在t时刻正反应速率等于逆反应速率
D.增大压强,一定能加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】5种物质已按沸点由低到高顺序排列),则正己烷最可能插入的位置是( )
① | ② | ③ | ④ | ⑤ |
甲烷 | 乙烯 | 戊烷 | 2-甲基戊烷 | 甲苯 |
A.③④之间B.②③之间C.④⑤之间D.⑤之后
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图![]() X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
(1)m=________,该融雪剂的化学式为________。
(2)Z、W元素的名称为________、_______。
(3)下列说法正确的是________。
A.XY2和WZ2都为离子化合物
B.XY2分子中仅含离子键,WZ2中仅含极性共价键
C.H2Z比HY的稳定性强
D.X的阳离子比Y的阴离子半径大
(4)下列化学用语表达正确的是________。
A.XY2的电子式:![]()
B.WZ2的结构式:Z=W=Z
C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-=2Y+Z↓
D.用电子式表示XY2的形成过程为:![]()
(5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,P、M、N均是由这些元素组成的二元化合物,它们存在转化关系Q![]() P+M+N,P能使湿润的红色石蕊试纸变蓝,M的组成元素位于同一主族,N常温常压下为液体。下列说法不正确的是
P+M+N,P能使湿润的红色石蕊试纸变蓝,M的组成元素位于同一主族,N常温常压下为液体。下列说法不正确的是
A. 原子半径:Y>Z>W>X
B. 简单气态氢化物的热稳定性:Z>Y
C. Q既能与强酸溶液反应,又能与强碱溶液反应
D. Y的最高价氧化物对应的水化物与Q溶液混合,无M生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同温度下,水溶液中c(H+)与c(OH-)的关系如下图所示。下列有关说法不正确的是( )
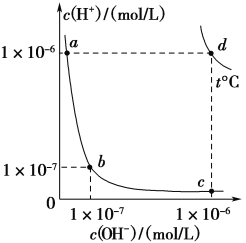
A. d点对应的食盐水pH=6,呈中性
B. 向a点对应的CH3COOH溶液中滴加NaOH溶液至b点,此时c(Na+)=c(CH3COO-)
C. 温度为t ℃时,0.05 mol/L Ba(OH)2溶液的pH=11
D. a点对应的稀硫酸与c点对应的CH3COONa溶液中水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙基环己烷常用作气相色谱对比样品,也用于有机合成。
(1)乙基环己烷(C8H16)脱氢制苯乙炔(C8H6)的热化学方程式如下:
①C8H16(l)![]() C8H10(l)+3H2(g) ΔH1>0
C8H10(l)+3H2(g) ΔH1>0
②C8H10(l)![]() C8H6(l)+2H2(g) ΔH2=a kJ·mol-1
C8H6(l)+2H2(g) ΔH2=a kJ·mol-1
③C8H6(l)+5H2(g)![]() C8H16(l) ΔH3=b kJ·mol-1
C8H16(l) ΔH3=b kJ·mol-1
则反应①的ΔH1为__________(用含a、b的代数式表示),有利于提高上述反应①的平衡转化率的条件是____(填字母)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)不同压强和温度下乙基环己烷的平衡转化率如下图所示。

①在相同压强下升高温度,未达到新平衡前,v正____(填“大于”“小于”或“等于”)v逆。
②研究表明,既升高温度又增大压强,C8H16(l)的转化率也升高,理由可能是____。
(3)t ℃,向恒容密闭反应器中充入1.00 mol C8H16(l)进行催化脱氢,测得液态C8H10(l)和C8H6(l)的产率x1和x2(以物质的量分数计)随时间变化关系如下图所示。

①在8 h时,反应体系内氢气的量为_____mol(忽略其他副反应),液态C8H16(l)的转化率是_________。
②x1显著低于x2的原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:
N2+ 3H2![]() 2NH3(正反应是放热反应)。下列有关说法正确的是( )
2NH3(正反应是放热反应)。下列有关说法正确的是( )
A. 降低温度可以加快反应速率
B. 达到化学反应限度时,生成2mol NH3
C. 向容器中再加入N2可以加快反应速率
D. 1mol N2和3mol H2的总能量低于2mol NH3的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,纤维素与乙酸酐反应可以制取醋酸纤维,同时还有乙酸生成,请写出化学方程式__________________________ ,化学反应类型_________________。已知某纤维乙酸酯的平均相对分子质量为311040,则对应的纤维素分子中平均含有的葡萄糖结构单元数(即聚合度n)是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com