
科目:高中化学 来源:2016-2017学年安徽省六安市高一上学期期末考试化学试卷(解析版) 题型:选择题
CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol·L-1, 则此溶液最多溶解铁粉的质量为( )
A. 5.6g B. 11.2g C. 22.4g D. 33.6g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省嘉峪关市高二上学期期末考试化学试卷(解析版) 题型:选择题
据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是 ( )
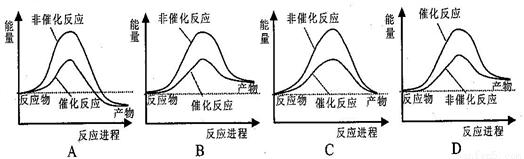
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省嘉峪关市高一上学期期末考试化学试卷(解析版) 题型:选择题
向25mL 18.4mo1·L-1 H2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量是( )
A. 小于0.23 mol B. 等于0.23 mol
C. 0.23mol~0.46mol之间 D. 等于0.46mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省嘉峪关市高一上学期期末考试化学试卷(解析版) 题型:选择题
证明某溶液含有Fe2+的实验方法是 ( )
A. 先滴加氯水,再滴加KSCN溶液后显红色
B. 先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C. 滴加NaOH溶液,产生白色沉淀
D. 只需滴加KSCN溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省新余市高二下学期入学考试化学试卷(解析版) 题型:填空题
下表为常见几种弱酸的电离常数,
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | HClO | 3×10-8 |
H2O2 | K1=2.4×10-12 K2=1×10-25 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
I.结合上表回答下列问题(均为常温下的数据):
(1)在常温下,相同物质的量浓度的①CH3COONa②Na2CO3③NaClO三种溶液的pH由小到大的顺序为______________________(用序号回答)
(2)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的钠盐,同时还有另两种钠盐生成,该反应的化学方程式为_________________
II.过氧化氢(H2 O2)为淡蓝色粘稠液体,是中学常见试剂.
(1)H2O2含有的共价键类型为_____________________
(2)实验室可用稀硫酸与BaO2反应来制取H2 O2,该反应的化学方程式为__________________
(3)经测定H2O2为二元弱酸,酸性比碳酸还弱,不稳定易分解.已知Na2O2中通人干燥的CO2不反应,但通人潮湿的CO2却可以产生O2,试用化学方程式表示这一过程___________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省新余市高二下学期入学考试化学试卷(解析版) 题型:选择题
室温下,下列溶液中粒子浓度关系正确的是( )
A. CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
B. Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S)
C. Na2CO3溶液:c(Na+)+c(H+)=2c(CO )+c(OH-)
)+c(OH-)
D. Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O )+2c(H2C2O4)
)+2c(H2C2O4)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高二2月月考化学试卷(解析版) 题型:选择题
铅蓄电池的电极材料是Pb和PbO2,电解质是硫酸溶液。现用铅蓄电池电解饱和硫酸钠溶液一段时间。已知蓄电池放电时发生的反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O,假设电解时温度不变且用惰性电极,下列结论不正确的是( )
A. 电解后,c(Na2SO4)不变,且溶液中有晶体析出
B. 电解池的阳极反应式为:4OH--4e-=2H2O+O2↑
C. 蓄电池电池放电时,每消耗0.1molPb,共生成0.1molPbSO4
D. 蓄电池中每生成2molH2O,电解池中就消耗1molH2O
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:简答题
用零价铁(Fe)进行水体脱氮、(去除水体中的NO3-),已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。其中作负极的物质是________,正极的电极反应式是_________。

(2)研究表明,零价铁脱氮后最终会在表面生成不导电的FeO(OH)外皮,从而使得脱氮过程停止。补充一定量的Fe2+可以明显提高NO3-的去除率。对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;Ⅱ. Fe2+破坏FeO(OH)氧化层。
针对假设I:做对比实验,结果如图所示,可得到的结论是_______。

②针对假设II:以同位素示踪法,证实Fe2+能与FeO(OH)反应生成Fe3O4。该反应的离子方程式为_______________,加入Fe2+提高NO3-去除率的原因:____________。
(3)将足量铁粉投入水体中,测定不同初始pH对脱氧的影响见下边左图,初始PH为2.5时氮浓度与pH变化见下边图。结合两图分析,不同初始pH对脱氮产生影响的原因为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com