
 H2O
H2O C2H4
C2H4 .
.  名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 )是制备氯丁橡胶的原料,它只比1,3-丁二烯(
)是制备氯丁橡胶的原料,它只比1,3-丁二烯( )多一个氯原子.但由于双键上的氢原子很难发生取代反应,不能通过1,3-丁二烯直接与氯气反应制得.2-氯-1,3-丁二烯的逆合成分析为:
)多一个氯原子.但由于双键上的氢原子很难发生取代反应,不能通过1,3-丁二烯直接与氯气反应制得.2-氯-1,3-丁二烯的逆合成分析为: $\stackrel{①}{→}$
$\stackrel{①}{→}$ $\stackrel{②}{→}$
$\stackrel{②}{→}$ $\stackrel{③}{→}$
$\stackrel{③}{→}$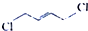 $\stackrel{④}{→}$
$\stackrel{④}{→}$ (提示:可利用1,3-丁二烯与Cl2的1,4-加成反应)
(提示:可利用1,3-丁二烯与Cl2的1,4-加成反应)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀硫酸的反应 | |
| B. | 木炭燃烧 | |
| C. | 甲烷在空气中燃烧的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
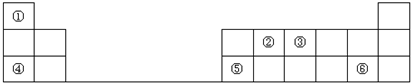
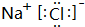
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液的酸性逐渐增强 | B. | 铜片逐渐溶解 | ||
| C. | 溶液中H+向锌片作定向移动 | D. | 锌片是负极并被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
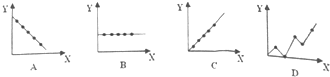
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤族元素是典型的非金属元素,因此不能与其他非金属元素反应 | |
| B. | 碱金属元素单质越活泼,其熔点和沸点就越高 | |
| C. | 卤族元素单质都能和氢气反应,且气态氢化物的稳定性随单质氧化性的增强而增强 | |
| D. | 卤族元素单质都能与水剧烈反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com