
【题目】化学与人类生产、生活密切相关。下列说法不正确的是( )
A.高纯度的硅单质广泛用于制作芯片
B.碳酸镁可用于制造耐高温材料氧化镁
C.SO2能用浓硫酸来干燥,说明其还原性不强
D.铁质地柔软,而生活中的钢质地坚硬,说明合金钢能增强铁的硬度
科目:高中化学 来源: 题型:
【题目】霾是空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成的视觉障碍,属于大气污染。如图为霾的主要成分示意图,下列说法不正确的是

A. 用丁达尔现象可以鉴别SO2和SO3的混合气体和有霾的空气
B. “光化学烟雾”“硝酸型酸雨”的形成与氮氧化合物有关
C. 苯、甲苯、二甲苯都属于芳香烃
D. SO2和NxOy都属于酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.分子式相同,各元素质量分数也相同的物质是同种物质
B.通式相同的不同物质一定属于同系物
C.分子式相同的不同物质一定是同分异构体
D.相对分子质量相同的不同物质一定是同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据方程式KClO3+6HCl=KCl+3Cl2↑+2H2O 回答下列问题
(1)氧化剂与还原剂的物质的量之比是:
(2)盐酸体现出的性质有:
(3)用双线桥表示出电子转移的方向和数目:KClO3+6HCl=KCl+3Cl2↑+2H2O
(4)当被氧化的HCl为73克时,转移的电子的数目为(填具体数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电子式的表述正确的是:
A. NaClO的电子式为![]()
B. SCl2的电子式为![]()
C. 用电子式表示HCl的形成过程为:H+![]() →
→![]()
D. 已知SCN-中每个原子都达到8电子结构,则其电子式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学组装了如图所示的电化学装置,电极Ⅰ为Zn,其他电极均为Cu。下列说法错误的是:
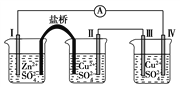
A. 电极Ⅰ发生氧化反应
B. 相同时间内,电极Ⅱ与电极Ⅳ的质量变化值相同
C. 电极Ⅲ的电极反应:4OH--4e-===O2↑+2H2O
D. 电流方向:电极Ⅳ→电流计→电极Ⅰ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32﹣)、c(HCO3﹣)都减少,其方法是( )
A.通入二氧化碳气体
B.加入氢氧化钠固体
C.通入氯化氢气体
D.加入饱和石灰水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要化合物,在工农业生产、生活中有着重要作用。
(1)“氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收制取硝酸(固定装置略去):
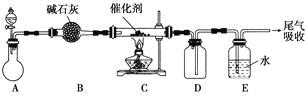
①A装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是________。
②C装置中发生反应的化学方程式为________________。
③反应后,装置E中除存在较多的H+外,还可能存在的一种离子是________,试设计实验证明这种离子的存在_____________________。
④下列哪些装置可以同时起到装置D和E的作用________(填代号)。
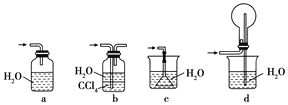
(2)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出反应的化学方程式:________________(不必配平),该反应生成的还原产物的化学键类型是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是重要的资源,可以制备一系列物质。下列说法正确的是
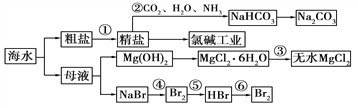
A. 步骤②中,应先通CO2,再通NH3
B. 除去粗盐中SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
C. 步骤③中可将MgCl2·6H2O晶体直接进行灼烧制得无水MgCl2
D. 步骤④、⑤、⑥反应中,溴元素均被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com