
Ⅰ.向Na2CO3溶液中滴入酚酞试液后溶液显红色,原因是(写离子方程式)_________。向上述溶液中滴入过量的CaCl2溶液,观察到的现象是__________________。
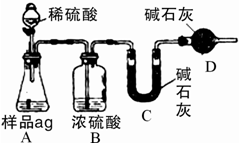
Ⅱ.某天然碱的组成为aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数)。现用下图所示装置(夹持仪器已略去)确定其组成,其中天然碱样品质量为

请回答:
(1)在用托盘天平称量样品时,如果天平指针向左偏转,说明_______________________。
(2)NaHCO3受热分解的化学反应方程式为________________________________________。
(3)E处碱石灰的作用是__________________________________________________。
(4)反应停止后打开活塞K,缓缓鼓入空气数分钟,该步骤的目的是__________________。
(5)实验结束后称得洗气瓶C质量增加
Ⅰ.![]() +H2O
+H2O![]()
![]() +OH- 产生白色沉淀,且溶液红色褪去
+OH- 产生白色沉淀,且溶液红色褪去
Ⅱ.(1)样品重于砝码
(2)2NaHCO3![]() Na2CO3+H2O+CO2↑(条件加热)
Na2CO3+H2O+CO2↑(条件加热)
(3)防止空气中的CO2和水蒸气进入U形管D中
(4)使反应产生的CO2和水蒸气被充分吸收
(5)Na2CO3·2NaHCO3·H2O
解析:Ⅰ.![]() +H2O
+H2O![]()
![]() +OH-,酚酞试液显红色,加过量CaCl2,Ca2++
+OH-,酚酞试液显红色,加过量CaCl2,Ca2++![]()
![]() CaCO3↓,溶液红色褪去.
CaCO3↓,溶液红色褪去.
Ⅱ.该实验通过测天然碱受热分解生成的CO2和H2O的质量,确定天然碱的成分.
洗气瓶C吸收样品分解生成的H2O,U形管D吸收NaHCO3分解生成的CO2.
(5)m总(H2O)=
2NaHCO3 ![]() CO2↑+H2O+Na2CO3
CO2↑+H2O+Na2CO3
2×
m(NaHCO3)=
所以
a:b:c=![]() =1:2:1
=1:2:1
即天然碱的化学式为Na2CO3·2NaHCO3·H2O.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
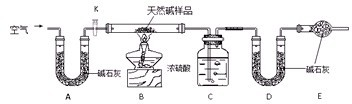
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 序号 | 甲 | 乙 | 丙 |
| 方案 | 用广泛pH试纸 检测溶液pH |
滴加等体积0.1mol?L-1 Ba(OH)2溶液 |
滴加等体积0.1mol?L-1 CaCl2溶液 |
| 0.01mol?L-1溶液 | NaHCO3 | Na2CO3 |
| c(CO32-)/mol?L-1 | 0.00011 | 0.0087 |
查看答案和解析>>
科目:高中化学 来源:2010—2011学年福建省福州市第八中学高一上学期期末考试化学试卷 题型:计算题
(11分)有一种白色粉末是无水碳酸钠和碳酸氢钠的混合物,称取4.42g灼烧至恒重,把放出的气体通入足量澄清石灰水中,生成2.00g沉淀,灼烧后的残渣能与30.0mL盐酸恰好完全反应。试求:
(1)原混合物中各物质的质量。 (2)所用盐酸的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省桐乡一中高一上学期期中考试化学试卷(带解析) 题型:计算题
(8分)有一种白色粉末是无水碳酸钠和碳酸氢钠的混合物,称取4.42g灼烧至恒重,把放出的气体通入足量澄清石灰水中,生成2.00g沉淀,灼烧后的残渣能与30mL盐酸恰好完全反应。试求:
(1)该白色粉末灼烧后产生气体在标准状况下的体积?
(2)原混合物中各物质的质量。
(3)所用盐酸的物质的量浓度。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com