
[ ]
科目:高中化学 来源: 题型:
A.对于有气体参与的平衡体系,若增大压强,使平衡向逆反应方向移动,则在新平衡前的逆反应速率大于正反应速率
B.对于气体的可逆反应,如果气体的平均相对分子质量保持不变时,则此可逆反应就达到了平衡状态
C.对于可逆反应达到平衡时,当增大反应物的浓度达到新的平衡时,则此反应物的转化率一定会提高
D.对于可逆反应:2NO2(g)![]() 2NO(g)+O2(g)达到平衡时,将各气体成分的浓度都增大一倍,则平衡向左移动
2NO(g)+O2(g)达到平衡时,将各气体成分的浓度都增大一倍,则平衡向左移动
查看答案和解析>>
科目:高中化学 来源:2015届广东省高二上学期期中考试理科化学试卷(解析版) 题型:选择题
从下列事实所得出的解释或结论正确的是
选项 实验事实 解释或结论
A 2N2O5(g) 4NO2(g)+O2(g) ΔH>0
4NO2(g)+O2(g) ΔH>0
在室温下能自发进行 这是一个熵增的反应
B 压缩针筒内的NO2和N2O4混合气体,
颜色先变深后变浅 增大压强,平衡向生成N2O4的方向移动,新平衡比旧平衡压强小
C 锌与稀硫酸反应过程中,开始反应后速率逐渐增大 该反应是放热反应
D 已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动 反应物的浓度一定降低
查看答案和解析>>
科目:高中化学 来源:深圳模拟 题型:多选题
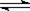
| A.将2molSO2和1molO2置于密闭容器中充分反应,放出热量为aKJ |
| B.压缩容器,正、逆反应速率都增大,平衡向正反应方向移动 |
| C.反应一段时间后,若混合气体的平均摩尔质量不变,则反应已达到平衡 |
| D.维持温度和容积不变,将反应物的浓度增大一倍,则平衡右移,平衡常数增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com