
| A、Cl-的浓度不变 |
| B、溶液变浑浊 |
| C、溶液中Al3+全部转化为AlO2- |
| D、溶液中存在最多的离子是Na+ |
| 4.6 |
| 23 |
| 0.2mol |
| 3 |
| 2 |
| 15 |


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
| A、电解MgCl2饱和溶液,可制得金属镁 |
| B、用食醋去除水壶中的水垢所发生的是水解反应 |
| C、在海轮外壳上镶入不活泼的铜块,可减缓船体的腐蚀速率 |
| D、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用作净化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、未冷却即转移、定容 |
| B、未洗烧杯及玻璃棒 |
| C、定容时俯视刻度线观察液面 |
| D、容量瓶中原有少量蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳的质量分数相同 |
| B、固态时均为分子晶体 |
| C、一定条件下能与H2发生加成反应,就一定能使KMnO4酸性溶液褪色 |
| D、C8H8可能含有苯环结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
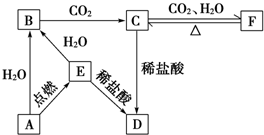 如图所示,下列各项变化的未知物焰色反应均呈黄色,E为淡黄色粉末.回答下列问题.
如图所示,下列各项变化的未知物焰色反应均呈黄色,E为淡黄色粉末.回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
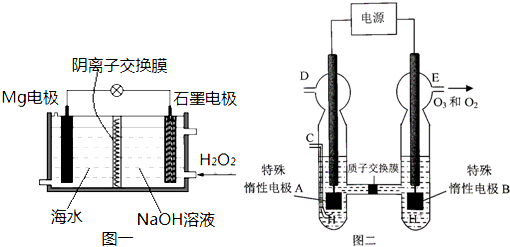
查看答案和解析>>
科目:高中化学 来源: 题型:
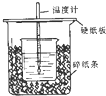 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com