
下列叙述正确的是( )
A.发生化学反应时失去电子越多的金属原子,还原能力越强
B.NaCl只有在水溶液中才能电离出Na +、Cl-
+、Cl-
C.能与酸反应的氧化物,不一定是碱性氧化物
D.电离时能产生H+的化合物是酸
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:选择题
用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得m(H):m(O)>1:8。下列对导致这一结果的原因的分析中,一定错误的是( )
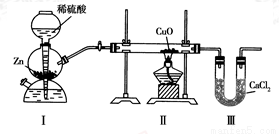
A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.CuO没有全部被还原
C.Ⅱ装置中玻璃管内有水冷凝
D.Ⅲ装置后缺少干燥装置
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省郏县一高、叶县二高等五校高二上期中化学卷(解析版) 题型:选择题
在25℃时将pH=11的NaOH溶液与pH=3的 的CH3COOH溶液等体积混合后,下列关系式中正确的是 ( )
A.c(Na+)=c(CH3COO-)+c(CH3COOH)
B.c(H+)=c(CH3COO-)+c(OH-)
C.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:实验题
某同学设计如下实验方案以分离KCl和BaCl2两种固体混合物,供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、硫酸、盐酸
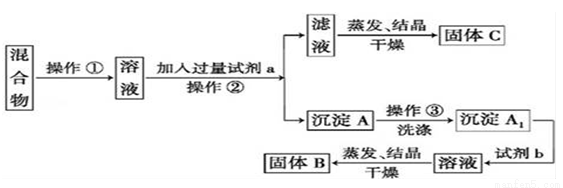
(1)操作①的名称是 ,操作②的名称是 。
(2)试剂a是 ,试剂b是 (填化学式)。
(3)加入试剂b所发生反应的离子方程式为 。
(4)该方案能否达到实验目的(填能或不能) .若不能,应如何改进(若能,此问不用回答) 。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是 。
A、固体C的质量 B、沉淀A的质量
C、沉淀A1的质量(未干燥) D、固体B的质量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:选择题
常温下,在溶液中可发生以下反应:
①H++Z-+XO42-→X2++Z2+H2O(未配平),②2M2++R2=2M3++2R-
③2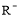 +Z2=R2+2
+Z2=R2+2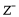 。由此判断下列说法正确的是
。由此判断下列说法正确的是
A.氧化性强弱顺序为XO42->Z2>R2>M3+
B.Z2在③中发生氧化反应
C.R元素在反应②中被氧化,在③中被还原
D.常温下反应不可进行2M2++Z2=2M3++2Z-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:选择题
下列各组物质中,含原子数最多的是( )
A.标准状况下5.6L 氢气 B.6.02×1022个H2SO4 C.11gCO2 D. 4℃时9mL水
C.11gCO2 D. 4℃时9mL水
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上学期期中化学试卷(解析版) 题型:填空题
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是______________,只有还原性的是____________,既有氧化性又有还原性的是______________。
(2)分析氧化还原反应2P+5Br2+8H2O=2H3PO4+10HBr,用“双线桥法”表示出反应中电子转移的方向和数目为_______________________。
反应中氧化剂与还原剂的物质的量之比为____________________。
(3) 氧化还原反应3S + 6KOH = K2S + K2SO3 + 3H2O中,氧化产物是______________,还原产物是_______________。该反应的离子方程式为:___________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上学期期中化学试卷(解析版) 题型:填空题
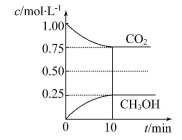
(1)在一定温度下的2 L固定容积的密闭容器中,通入2 mol CO2和3 mol H2,发生的反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-akJ·mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-akJ·mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
①能说明该反应已达平衡状态的是_____________(填编号)。
A.单位时间内每消耗1.2 mol H2,同时生成0.4 mol H2O
B.CO2的体积分数在混合气体中保持不变
C.混合气体的平均相对分子质量不随时间的变化而变化
D.该体系中H2O与CH3OH的物质的量浓度之比为1∶1,且保持不变
②若要使K=1,则改变的条件可以是_____________(填选项)。
A增大压强 B减小压强 C升高温度 D降低温度 E加入催化剂
(2)有一种用CO2生产甲醇燃料的方法。已知:
CO2(g)+3H2(g) CH3OH(g)+H2O(l) ΔH=-akJ·mol-1;
CH3OH(g)+H2O(l) ΔH=-akJ·mol-1;
CH3OH(g)=CH3OH(l) ΔH=-bkJ·mol-1;
2H2(g)+O2(g)=2H2O(l) ΔH=-ckJ·mol-1;
则表示CH3OH(l)燃烧热的热化学方程式为 。
(3)在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g) 3C(g)+2D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。
3C(g)+2D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高。
物质 | A | B | C | D |
起始投料/mol | 2 | 1 | 3 | 0 |
该反应的平衡常数表达式为K=__________。升高温度,平衡常数将__________(填“增大”“减小”或“不变”)。
(4)为研究不同条件对反应2NO(g)+Cl2(g) 2ClNO(g) ΔH<0的影响,在恒温下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应达到平衡,测得NO的转化率为α1;其他条件保持不变,反应在恒压条件下进行,达到平衡时NO的转化率为α2,则α1________α2(填“大于”“小于”或“等于”)。
2ClNO(g) ΔH<0的影响,在恒温下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应达到平衡,测得NO的转化率为α1;其他条件保持不变,反应在恒压条件下进行,达到平衡时NO的转化率为α2,则α1________α2(填“大于”“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高二上学期期中化学试卷(解析版) 题型:选择题
在0.1mol/L醋酸的溶液中,加入水会使下列比值增大的是( )
A.c(CH3COOH)/c(CH3COO—) B.c(CH3COO—)/c(OH—)
C.c(H+)/c(CH3COOH) D.c(H+)/ c(OH—)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com