
常温下,一定浓度的某溶液,由水电离出的c(OH﹣﹣)=10﹣﹣4mol/L,则该溶液中的溶质可能是()
A. Na2SO4 B. CH3COOH C. NaOH D. CH3COOK
考点: 水的电离;盐类水解的应用.
专题: 电离平衡与溶液的pH专题.
分析: 常温下,水的离子积为:10﹣14,由水电离出的c(OH﹣)=10﹣4mol/L,c(H+)•c(OH﹣)=10﹣8>10﹣14,水的电离程度增大,说明所加的溶质促进水的电离,结合选项知,只能是水解呈碱性的强碱弱酸盐醋酸钠.
解答: 解:常温下,由水电离出的c(OH﹣)=10﹣4mol/L,水电离的氢离子浓度等于氢氧根离子浓度,则c(H+)•c(OH﹣)=10﹣8>10﹣14,说明该溶液中溶质促进了的水的电离,硫酸、氢氧化钠、硫酸氢钾都抑制了水的电离,只有醋酸钠属于强碱弱酸盐,醋酸根离子结合水电离的氢离子,促进了水的电离,
故选D.
点评: 本题考查了水的电离、盐的水解等知识,题目难度中等,试题侧重对学生灵活运用基础知识解决实际问题的能力的培养,解题的关键是准确判断出溶液中的溶质对水的电离程度的影响.


科目:高中化学 来源: 题型:
下图所示的实验,能达到实验目的是()
A. 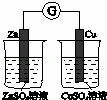
验证化学能转化为电能 B. 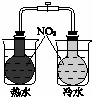
证明温度对平衡移动的影响
C. 
验证铁发生析氢腐蚀 D. 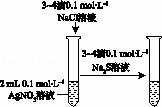 验证AgCl溶解度大于Ag2S
验证AgCl溶解度大于Ag2S
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)⇌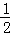 N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是()
N2(g)+CO2(g)△H=﹣373.2kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是()
A. 加催化剂同时升高温度 B. 加催化剂同时增大压强
C. 升高温度同时充入N2 D. 降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
T℃时,有甲、乙两个密闭容器,甲容器的体积为1L,乙容器的体积为2L,分别向甲、乙两容器中加入6mol A和3mol B,发生反应如下:3A(g)+bB(g)⇌3C(g)+2D(g)△H<0; 4min时甲容器内的反应恰好达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L; t min时乙容器内的反应达平衡,根据题给信息回答下列问题:
(1)甲容器中反应的平均速率v(B)= ,化学方程式中计量数b= .
(2)乙容器中反应达到平衡时所需时间t 4min(填“大于”、“小于”或“等于”).
(3)若要使甲、乙容器中B的平衡浓度相等,可以采取的措施是AC.
A.保持温度不变,增大甲容器的体积至2L
B.保持容器体积不变,使甲容器升高温度
C.保持容器压强和温度都不变,向甲中加入一定量的A气体
D.保持容器压强和温度都不变,向甲中加入一定量的B气体
(4)写出平衡常数表达式K= ,并计算在T℃时的化学平衡常数K .
查看答案和解析>>
科目:高中化学 来源: 题型:
关于浓度均为0.1mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是()
A. c(NH+4):③>①
B. 水电离出的c(H+):②>①
C. ①和②等体积混合的溶液:c(H+)=c(OH﹣)+c(NH3•H2O)
D. ①和③等体积混合后的溶液:c(NH+4)>c(Cl﹣)>c(OH﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下体积相同的下列四种溶液:①pH=3的盐酸②pH=3的醋酸溶液③pH=11的氨水④pH=11的NaOH溶液.下列说法中,正确的是()
A. ②和④混合,所得混合溶液的pH大于7
B. 将四种溶液分别稀释到体积为原的100倍,溶液pH大小顺序③>④>②>①
C. ③和④分别与足量稀硫酸中和,消耗硫酸的体积③=④
D. ①和③混合,所得混合溶液中c(H+)+c(NH4+)=c(Cl﹣)+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
工业废水中常含有一定量的Cr2O72﹣和CrO42﹣,它们会对人类及生态系统产生很大的伤害,必须进行处理.某工厂使用还原沉淀法处理,该法的工艺流程为:CrO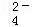
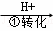 CrO
CrO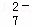
 Cr3+
Cr3+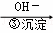 Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42﹣(黄色)+2H+⇌Cr2O72﹣(橙色)+H2O
(1)若平衡体系的pH=12,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 .
a.Cr2O72﹣的浓度不变 b.Cr2O72﹣和CrO42﹣的浓度相同c.2v(Cr2O72﹣)=v(CrO42﹣)d.溶液的颜色不变
(3)第②步反应中,还原剂为 .
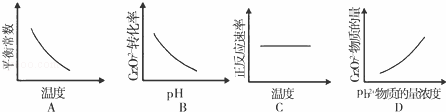
(4)电镀废液中Cr2O72﹣还可通过下列反应转化:
Cr2O72﹣(aq)+2Pb2+(aq)+H2O(l)⇌2PbCrO4(s)+2H+(aq)△H<0
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是A
(5)泡沫灭火器中所用的原料是小苏打(NaHCO3)和硫酸铝,写出泡沫灭火器中当两者混合时发生反应的离子方程式 .
(6)已知NaHSO3溶液显酸性,其原因是 (用离子方程式和相关语言说明)
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式如图所示,关于该物质的叙述错误的是( )
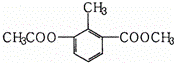
A. 一个分子中含有12个H原子
B. 能使酸性KMnO4溶液褪色
C. 苯环上的一氯代物有2种
D. 1mol该物质分别与足量H2、NaOH溶液反应,消耗其物质的量均为3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42﹣、NO3﹣、Cl﹣,该溶液放在用惰性材料做电极的电解槽中,通电片刻后,则氧化产物与还原产物的质量之比为()
A. 35.5:108 B. 16:207 C. 8:1 D. 108:35.5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com