
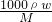 公式变形计算硫酸的质量分数,结合硫酸溶液的浓度越大密度越大,进行判断;
公式变形计算硫酸的质量分数,结合硫酸溶液的浓度越大密度越大,进行判断;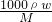 计算硫酸的浓度,结合浓硫酸溶液的浓度越大密度越大,进行判断.
计算硫酸的浓度,结合浓硫酸溶液的浓度越大密度越大,进行判断.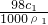 ,ω2=
,ω2=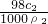 ,所以
,所以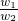 =
=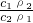 =
=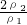 ,浓硫酸的浓度越大密度越大,则ρ1>ρ2,故ω1<2ω2,稀释前后溶质的质量不变,所以稀释后溶液的质量小于100g,故水的质量小于50g,水的密度为1g/ml,所以水的体积V<50ml;故A正确;
,浓硫酸的浓度越大密度越大,则ρ1>ρ2,故ω1<2ω2,稀释前后溶质的质量不变,所以稀释后溶液的质量小于100g,故水的质量小于50g,水的密度为1g/ml,所以水的体积V<50ml;故A正确;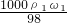 ,c2=
,c2=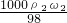 ,所以
,所以 =
=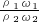 =
=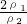 ,浓硫酸的浓度越大密度越大,则ρ1>ρ2,故c1>2c2,故C错误;
,浓硫酸的浓度越大密度越大,则ρ1>ρ2,故c1>2c2,故C错误;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013届浙江省余姚中学高三上学期期中考试化学试卷(带解析) 题型:单选题
将50g质量分数为ω1,物质的量浓度为C1的浓硫酸沿玻璃棒加入到VmL水中,稀释后得到质量分数为ω2,物质的量浓度为C2的稀溶液。下列说法中正确的是
| A.若ω1=2ω2,则C1<2C2,V=50mL | B.若C1=2C2,则ω1<2ω2,V>50mL |
| C.若C1=2C2,则ω1<2ω2,V<50mL | D.若ω1=2ω2,则C1>2C2,V<50ml |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省高三上学期期中考试化学试卷(解析版) 题型:选择题
将50g质量分数为ω1,物质的量浓度为C1的浓硫酸沿玻璃棒加入到VmL水中,稀释后得到质量分数为ω2,物质的量浓度为C2的稀溶液。下列说法中正确的是
A.若ω1=2ω2,则C1<2C2,V=50mL B.若C1=2C2,则ω1<2ω2,V>50mL
C.若C1=2C2,则ω1<2ω2,V<50mL D.若ω1=2ω2,则C1>2C2,V<50ml
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com