
| A. | 标准状况下,22.4L苯含有NA个苯分子 | |
| B. | 0.2 mol•L-1 FeCl3溶液中含有Cl-总数为0.6NA | |
| C. | 在标准状况下,含4molHCl的浓盐酸与足量的MnO2反应可生成22.4L氯气 | |
| D. | 4g氦气所含分子数为NA |
分析 A、标况下,苯为液体;
B、溶液体积不明确;
C、MnO2只能与浓盐酸反应,一旦浓盐酸变稀,则反应即停止;
D、氦气是单原子分子,摩尔质量为4g/mol.
解答 解:A、标况下,苯为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、溶液体积不明确,故溶液中的氯离子的个数无法计算,故B错误;
C、MnO2只能与浓盐酸反应,一旦浓盐酸变稀,则反应即停止,则4molHCl不能完全反应,则生成的氯气的物质的量小于1mol,即在标况下小于22.4L,故C错误;
D、氦气是单原子分子,摩尔质量为4g/mol,故4g氦气的物质的量n=$\frac{4g}{4g/mol}$=1mol,故含有NA个分子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的运用以及物质的状态和结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题

 ;其所含化学键类型为共价键、离子键;
;其所含化学键类型为共价键、离子键;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用A表示的反应速率是0.4mol•L-1•min-1 | |
| B. | 分别用B、C、D表示的反应速率其比值为3:2:1 | |
| C. | 在2min末的反应速率,用B表示是0.3mol•L-1•min-1 | |
| D. | 在2min内用B表示的反应速率的值是逐渐减小的,用C表示的反应速率的值是逐渐增大的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 消去-取代-加成 | B. | 取代-消去-加成 | C. | 消去-加成-水解 | D. | 水解-取代-取代 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Z<Y<W,而离子半径:W<Y<Z | |
| B. | 含W的盐溶液一定呈酸性 | |
| C. | 由X、Y、Z组成的盐的水溶液呈酸性,则溶液中该盐阳离子浓度大于酸根离子浓度 | |
| D. | W和Y形成的原子个数比为1:1的共价化合物,具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域,是一种原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=2的HA溶液与pH=12的MOH溶液以任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) | |
| B. | pH=10的Na2A溶液中:2 c(Na+)=c(HA-)+c(H2A)+c(A2-) | |
| C. | 等物质的量浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| D. | 氨水和氯化铵的混合溶液,可能会出现c(NH${\;}_{4}^{+}$)>c(Cl-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA | |
| B. | 标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA | |
| C. | 0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| D. | 标准状况下,22.4L苯中C-H键数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜电极上发生还原反应 | |
| B. | 电池工作时,铜电极附近会出现蓝色 | |
| C. | 锌片失去的电子通过番茄汁流向铜电极 | |
| D. | 工作一段时间后,两极质量均减轻 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
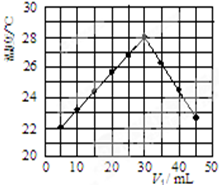 (一)实验方法测定反应热---------中和热测定
(一)实验方法测定反应热---------中和热测定| 实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1Cl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com