
| A. | 升高温度,正反应速率增加,逆反应速率减小 | |
| B. | 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 | |
| C. | 升高温度有利于反应速率增加,从而缩短达到平衡的时间 | |
| D. | 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
分析 该反应为气体体积减小、放热的反应,升高温度,正逆反应速率加快,平衡逆向移动,但增大或减小压强,正逆反应速率同等程度的变化,平衡不移动,以此来解答.
解答 解:A.升高温度,正逆反应速率均增大,且逆反应速率大于正反应速率,故A错误;
B.该反应为气体体积减小、放热的反应,升高温度,平衡逆向移动,增大压强平衡正向移动,故B错误;
C.升高温度,反应速率加快,从而缩短达到平衡的时间,故C正确;
D.该反应为放热反应,降低温度平衡正向移动,减小压强平衡逆向移动,故D错误;
故选C.
点评 本题考查化学平衡的移动,为高频考点,把握温度、压强对反应速率及化学平衡的影响为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 该实验过程中要用到氧化剂 | |
| B. | 检验碘单质是否存在,可用碘化钾溶液 | |
| C. | 要萃取碘水中的碘,可以用汽油或酒精 | |
| D. | 利用如图所示装置不能分离食盐和晶体碘的混和物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
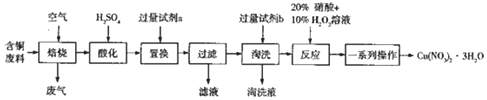
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氯化钡溶液中通入少量CO2 | |
| B. | 向饱和氢氧化钠溶液中加入钠单质 | |
| C. | 向饱和碳酸钠溶液中通入过量CO2 | |
| D. | 向NaHCO3溶液中加入过量澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | AlCl3 | B. | NaHCO3 | C. | Na2CO3 | D. | Al2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
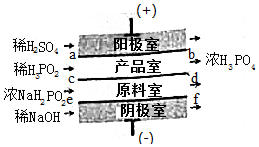 次磷酸(H3PO2)位一元酸,具有较强的还原性.可利用NaH2PO2为原料,通过四室电渗析法制备,工作原理如图所示,采用惰性电极,ab,cd,ef均为只允许阳离子(或阴离子)通过的离子交换膜,分别称为阳膜(或阴离子),下列说法描述错误的是( )
次磷酸(H3PO2)位一元酸,具有较强的还原性.可利用NaH2PO2为原料,通过四室电渗析法制备,工作原理如图所示,采用惰性电极,ab,cd,ef均为只允许阳离子(或阴离子)通过的离子交换膜,分别称为阳膜(或阴离子),下列说法描述错误的是( )| A. | 阳极室反应为:2H2O-4e-=O2↑+4H+ | |
| B. | ab,ef均为阳膜,cd为阴膜 | |
| C. | 若将稀H2SO4改为H3PO3,撤去ab膜,产品中总混有杂质的原因是:H3PO2在阳极放电而被氧化生成H3PO4 | |
| D. | 通电后产品室中的H+离子向原料室迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
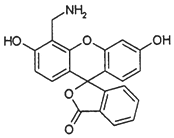
| A. | 分子中三个苯环处于同一平面 | |
| B. | 1 mol 4-AFMF 最多可与2molNaOH 反应 | |
| C. | 在酸性条件下水解,水解产物只有1种 | |
| D. | 能与溴水、FeCl3溶液及稀硫酸发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com