
| A£® | Fe”śFeCl2 | B£® | Na”śNa2O2 | C£® | S”śSO3 | D£® | N2”śNO2 |
·ÖĪö A£®ĀČĘų¾ßÓŠĒæŃõ»ÆŠŌ£»
B£®NaČ¼ÉÕÉś³É¹żŃõ»ÆÄĘ£»
C£®SČ¼ÉÕÉś³É¶žŃõ»ÆĮņ£»
D£®µŖĘųÓėŃõĘųŌŚ·Åµē»ņøßĪĀĻĀÉś³ÉNO£®
½ā“š ½ā£ŗA£®FeÓėĀČĘųÖ±½Ó»ÆŗĻÉś³ÉFeCl3£¬¹ŹA²»Ń”£»
B£®NaÓėŃõĘų¼ÓČČ·“Ó¦Ö±½Ó»ÆŗĻÉś³ÉNa2O2£¬¹ŹBŃ”£»
C£®SÓėŃõĘųÖ±½Ó»ÆŗĻÉś³ÉSO2£¬¹ŹC²»Ń”£»
D£®µŖĘųÓėŃõĘųÖ±½Ó»ÆŗĻÉś³ÉNO£¬¹ŹD²»Ń”£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲ»ÆŗĻĪļŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĪļÖŹµÄŠŌÖŹ”¢·¢ÉśµÄ·“Ó¦ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
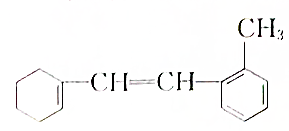 [µäŠĶĄżĢā”Ģijӊ»śĪļµÄ½į¹¹¼ņŹ½ČēĶ¼£ŗ
[µäŠĶĄżĢā”Ģijӊ»śĪļµÄ½į¹¹¼ņŹ½ČēĶ¼£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »ģŗĻĘųĢåµÄŃ¹Ēæ²»ŌŁøıä | |
| B£® | ĘųĢåCŌŚ»ģŗĻĘųĢåÖŠĖłÕ¼µÄĪļÖŹµÄĮæ·ÖŹż²»ŌŁøıä | |
| C£® | »ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁøıä | |
| D£® | µ„Ī»Ź±¼äÄŚĻūŗÄn mol CµÄĶ¬Ź±ĻūŗÄ2n mol A |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3 mol•L-1HCl | B£® | 4 mol•L-1HNO3 | ||
| C£® | 8 mol•L-1NaOH | D£® | 18 mol•L-1ÅØH2SO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4·Ö×ӵıȥżÄ£ŠĶ£ŗ | B£® | 2-¼×»ł-1£¬3-¶”¶žĻ©µÄ¼üĻߏ½  | ||
| C£® | ŅŅČ²·Ö×ӵĵē×ÓŹ½£ŗH£ŗC©«©«C£ŗH | D£® | ŅŅĻ©µÄ½į¹¹¼ņŹ½£ŗCH2CH2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | lmol OHŅ»ÖŠŗ¬ÓŠ9 NAøöµē×Ó | |
| B£® | 46g NO2ŗĶN2O4»ģŗĻĪļÖŠĖłŗ¬Ō×ÓŹżÄæĪŖ3NA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ50g 46%µÄŅŅ“¼ČÜŅŗÖŠ£¬Ėłŗ¬ŃõŌ×ÓŹżÄæĪŖ0.5NA | |
| D£® | .³£ĪĀĻĀ£¬56gĢś·ŪÓė×ćĮæÅØĻõĖį·“Ó¦£¬µē×Ó×ŖŅĘŹżÄæŠ”ÓŚ3NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ×å ÖÜĘŚ | IA | O | ||||||
| 1 | ¢Ł | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | |
| 2 | ¢Ś | ¢Ū | ¢Ü | |||||
| 3 | ¢Ż | ¢Ž | ¢ß | ¢ą | ||||
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ĻņAl2£ØSO4£©ČÜŅŗÖŠÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗŹ±£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæyÓė¼ÓČėBa£ØOH£©2µÄĪļÖŹµÄĮæxµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬×ŹĮĻ±ķĆ÷Ba£Ø AlO2£©2æÉČÜÓŚĖ®£®ĻĀĮŠÓŠ¹ŲŠšŹö“ķĪóµÄŹĒ£Ø””””£©
ĻņAl2£ØSO4£©ČÜŅŗÖŠÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗŹ±£¬Éś³É³ĮµķµÄĪļÖŹµÄĮæyÓė¼ÓČėBa£ØOH£©2µÄĪļÖŹµÄĮæxµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬×ŹĮĻ±ķĆ÷Ba£Ø AlO2£©2æÉČÜÓŚĖ®£®ĻĀĮŠÓŠ¹ŲŠšŹö“ķĪóµÄŹĒ£Ø””””£©| A£® | Ļ߶Īob£ŗAl£ØOH£©3³ĮµķŗĶBaSO4³Įµķ¹²“ę | |
| B£® | Ļ߶Īcd£ŗČÜŅŗÖŠn£ØAlO2£©£¾£ØBa2+£© | |
| C£® | Ļ߶Īad£ŗn£ØBaSO4£©”Żn[Al£ØOH£©3] | |
| D£® | Ļ߶Īde£ŗČÜŅŗÖŠn£ØBa2+£©Ź¼ÖÕ²»µČÓŚn£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com