
下列离子方程式的书写正确的是
A、铁和稀硫酸反应:2Fe + 6H+ =2Fe 3+ +3H 2↑
B、钠和冷水反应 Na+2H2O=Na++2OH?+H2↑
C、氢氧化钡溶液与稀 H2SO4 反应:Ba2++2OH―+SO42-+2H+=BaSO4↓+2H2O
D、NaHCO3溶液与Ca(OH)2溶液反应: OH― + HCO3- = CO32-+ H2O
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:2016届湖南省高三上学期月考化学试卷(解析版) 题型:选择题
下列有关物质分类或归类正确的是
① 混合物:盐酸、氯水、水银
② 化合物:CaCl2、NaOH 、HD
③ 电解质:胆矾、冰醋酸、氯化银
④ 同素异形体:C60、金刚石、石墨
⑤ 放热反应:盐酸与氢氧化钠、碳与二氧化碳高温化合成一氧化碳、甲烷燃烧
A.①③ B.②③ C.③④ D.④⑤
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上四次模拟化学卷(解析版) 题型:选择题
下列与NaHSO3溶液有关的离子方程式书写错误的是
A.NaHSO3溶液与FeCl3反应:HSO3-+2 Fe3++H2O=SO42-+2Fe2++3H+
B.NaHSO3溶液和足量Ca(OH)2溶液反应:Ca2++OH-+HSO3-=CaSO3↓+H2O
C.NaHSO3溶液和稀HNO3反应:HSO3-+H+=SO2↑+H2O
D.NaHSO3溶液和NaAlO2溶液反应:HSO3-+ AlO2-+H2O=SO32-+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源:2016届山东省北校高三上学期第二次单元测试化学试卷(解析版) 题型:填空题
甲醇是一种很好的燃料,工业上可用多种原料通过不同的反应制得甲醇.
(1)已知在常温常压下:
CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=﹣442.8kJ•mol﹣1
2CO(g)+O2(g)=2CO2(g)△H=﹣566.0kJ•mol﹣1
H2O(g)=H2O(l)△H=﹣44.0kJ•mol﹣1
则2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=
(2)已知C(s)+H2O(g)=CO(g)+H2(g) ΔH =akJ·mol-1
=akJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为____________________
(3)工业上正在研究利用来生产甲醇燃料的方法,该反应为:
CO2(g)+3H2(g)? CH3OH(g)+H2O(g)△H=﹣49.0kJ•mol﹣1
在某温度下,将6mol CO2和8mol H2充入容积为2L的密闭容器中,8分钟时达平衡状态,H2的转化率为75%.请回答:
①用CH3OH表示该反应在0﹣8min内的平均反应速率v(CH3OH)= .
②此温度下该反应平衡常数K= ;
(4)一氧化碳与氢气也可以合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H<0
①若该反应在恒温恒容条件下进行,下列说法正确的是 ;
a.若混合气体的密度不再改变,说明反应已达化学平衡状态
b.反应达到平衡后,通入CH3OH(g)使压强增大,平衡向右移动
c.反应达到平衡后,通入氩气使压强增大,平衡向右移动
d.反应达到平衡后,升高温度,平衡逆向移动,平衡常数减小
e.若使用催化剂,会改变反应的途径,但反应热不变
②某温度下,在一个容积为2L的密闭容器中进行该反应,已知此温度下的平衡常数K=50L2•mol﹣2,反应到某时刻测得各组分的物质的量如下:
物质 | CO | H2 | CH3OH |
物质的量/(mol) | 0.4 | 0.4 | 0.8 |
请比较此时正、逆反应速率的大小:v正 v逆(填“>”、“<”或“=”).
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省宜春市高一上学期第三次月考化学试卷(解析版) 题型:选择题
金属钠分别投入下列溶液中,放出气体且最终不一定有沉淀的是
A.MgCl2溶液 B.CuSO4溶液
C.FeCl3溶液 D.Al2(SO4)3溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二上学期第一次质检化学试卷(解析版) 题型:选择题
分别用X、Y、Z、W四种金属进行如下三个实验:
1 | 将X与Y用导线连接,浸入电解质溶液中,Y不易腐蚀 |
2 | 将X、W分别投入等浓度的稀盐酸中都有气体产生,但W比X反应剧烈 |
3 | 用惰性电极电解含等物质的量浓度的Y2+和Z2+混合溶液,在阴极上首先析出单质Z |
根据以上事实的下列判断错误的是
A.Z的阳离子氧化性最强
B.W的还原性强于Y的还原性
C.Z放入CuSO4溶液中一定有Cu析出
D.用X、Z和稀硫酸构成的原电池,X做负极
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西省高二上段考文化学试卷(解析版) 题型:选择题
科学家正在研究开发新的能源。“绿色能源”目前是研究的新能源之一,高粱、玉米等植物的种子经发酵、蒸馏就可以得到一种“绿色能源”物质。这种物质是
A.氢气 B.甲烷 C.酒精 D.木炭
查看答案和解析>>
科目:高中化学 来源:2015-2016年陕西西藏民族学院附属中学高二上期末化学卷(解析版) 题型:选择题
已知溶液中存在平衡:Ca(OH)2 (s) 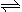 Ca2+(aq)+2OH-(aq) ΔH<0。下列有关该平衡体系的叙述正确的是( )
Ca2+(aq)+2OH-(aq) ΔH<0。下列有关该平衡体系的叙述正确的是( )
A.升高温度,固体的量减少
B.加入少量Na2CO3粉末能增大钙离子的浓度
C.降低温度,溶液中c(OH-)增大
D.恒温下加入少量CaO,溶液的pH增大
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三上一轮复习检测二化学试卷(解析版) 题型:选择题
用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
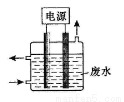
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H2O
C.阴极的电极反应式为:2H2O + 2e- = H2↑ + 2OH-
D.除去CN-的反应:2CN-+ 5ClO- + 2H+ = N2↑ + 2CO2↑ + 5Cl-+ H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com