
【题目】下列除去杂质的方法中错误的是( )
物质 | 杂质 | 除杂质的方法 | |
A | SiO2 | CaCO3 | 过量稀硫酸、过滤 |
B | 铜粉 | 铝粉 | 过量CuCl2溶液、过滤 |
C | FeCl3溶液 | FeCl2 | 通入适量氯气 |
D | SO2 | HC1 | 通过NaHSO3溶液的洗气瓶 |
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法不正确的是

A. 线段Ⅱ表示Fe2+的变化情况
B. 线段Ⅳ发生反应的离子方程式为:I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O
C. 根据图象可计算a=6
D. 原溶液中c(Fe2+)∶c(I-)∶c(Br-)=2∶1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【题目】有机物E是医药合成中间体.其合成路线如图:
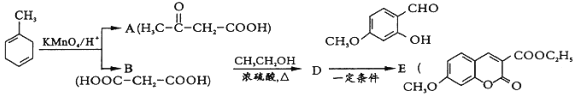
(1)![]() 的官能团名称为______.
的官能团名称为______.
(2)已知![]() 的系统命名为 2-丙酮酸,则A的名称是________________.
的系统命名为 2-丙酮酸,则A的名称是________________.
(3)D为二元酯,则B→D的化学方程式为________________________________________.
D→E的反应历程如图:

(4)写出这几步的反应类型:I_____________,Ⅱ____________III____________
(5)![]() 中能与稀 NaOH溶液反应的官能团是______.检验该官能团的方法是__________________________________________.
中能与稀 NaOH溶液反应的官能团是______.检验该官能团的方法是__________________________________________.
(6)写出满足下列条件的D的所有同分异构体的结构简式______________________________.
a.核磁共振氢谱有3组峰
b.常温下能与NaHCO3按1:2反应并释放出气体
(7)由化合物A经过两步便可以合成环境友好型高聚物聚3-羟基丁酸酯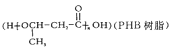
请写出反应合成线路,结合已知信息选用必要的无机试剂,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)的机械强度高,抗蚀能力强,有“未来金属”之称。工业上常用硫酸浸钛铁矿(其主要成分为钛酸亚铁(FeTiO 3它难溶于水,但能与酸反应)的方法制取二氧化钛 ,再由二氧化钛 制取金属钛。工艺流程如下:

回答下列问题
(1) FeTiO3中钛元素的化合价为____。
(2)稀硫酸与FeTiO3反应的离子方程式为:____。
(3)过程V表现了金属镁的还原性比金属钛的还原性____(填“强”或“弱”)。
(4)写出过程IV的化学方程式____(注意焦炭过量)。
(5)酸浸中,铁的浸出率与时间、温度的关系如图所示,如图可知,当铁的浸出率为70%时,可采用的实验条件为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.海水晒盐后所得的苦卤中含有较高浓度的MgCl2、KCl以及金属溴化物。以下是苦卤化学分离的过程。
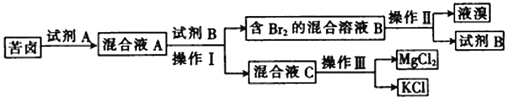
回答下列问题:
(1)若试剂A是一种有色气体单质,则A是_______(填化学式);
(2)“操作II”是_______,“操作III”是_______。(填字母)
a.蒸发 b.蒸馏 c.分液 d.重结晶
(3)试剂B可能是下列物质中的________。(填字母)
a.饱和NaCl溶液 b.CCl4 c.NaOH d.乙醇
Ⅱ.一种工业制备SrCl2·6H2O的生产流程如下图所示:

已知:①M(SrCl2·6H2O)=267g·mol-1;②Ksp(SrSO4)=3.3×10-7、Ksp(BaSO4)=1.1×10-10;③经盐酸浸取后,溶液中有Sr2+和Cl-及少量Ba2+。
(1)加入硫酸溶液的目的是______________;为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol·L1 (注:此时滤液中Ba2+浓度为1×105 mol·L1)。
(2)产品纯度检测:称取1.000 g产品溶解于适量水中,向其中加入含AgNO3 1.100×102 mol的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应的离子),待Cl-完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol·L1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_________________________________________。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为_______(保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下试剂的保存方法,其中不能用氧化还原反应解释的是( )
A. 钠保存在煤油中 B. 氯水保存在棕色的试剂瓶中
C. 保存FeSO4溶液需加入少量铁粉 D. 盛装NaOH溶液的试剂瓶不能用玻璃塞
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com