
| A. | 无色溶液中:K+、Na+、Cu2+、SO42- | |
| B. | Kw/c(OH-)=10-12 mol•L-1的溶液:Na+、K+、SiO32-、Cl- | |
| C. | 0.1 mol•L-1FeSO4溶液中:K+、NH4+、MnO4-、ClO- | |
| D. | 使酚酞变红色的溶液:Na+、Ba2+、NO3-、Cl- |
分析 A.Cu2+为蓝色;
B.Kw/c(OH-)=10-12 mol•L-1的溶液,显碱性;
C.离子之间发生氧化还原反应;
D.使酚酞变红色的溶液,显碱性.
解答 解:A.Cu2+为蓝色,与无色不符,故A不选;
B.Kw/c(OH-)=10-12 mol•L-1的溶液,显碱性,该组离子之间不反应,可大量共存,故B选;
C.MnO4-、ClO-分别与Fe2+发生氧化还原反应,不能共存,故C不选;
D.使酚酞变红色的溶液,显碱性,该组离子之间不反应,可大量共存,故D选;
故选BD.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:选择题
| A. | MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 医疗上用的“钡餐”其成分是碳酸钡,漂白粉的成分为次氯酸钙 | |
| D. | “海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{83}^{209}$Bi 和${\;}_{83}^{210}$Bi都含有83个中子 | |
| B. | 同位素:H2、D2、T2 | |
| C. | H2O和NH3分子中具有相同的质子数和电子数 | |
| D. | 稀有气体的原子最外层都达到8电子稳定结构,故都不能与别的物质发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
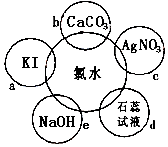 (1)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):
(1)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量): .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | 在c(H+)=1×10-13mol•L-1的溶液中:Na+、Fe3+、Cl-、SO42-能大量共存 | |
| C. | 铜溶于FeCl3溶液中:Cu+Fe3+=Fe2++Cu2+ | |
| D. | 向溶液中加入BaCl2溶液后再加盐酸,有白色沉淀,说明该溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
下列离子方程式与所述事实相符且正确的是
A.向FeBr2溶液中通入过量的Cl2:2Fe2++2Br-+2Cl2===2Fe3++Br2+4Cl-
B.用食醋除去水壶内的水垢:CaCO3+2H+ = Ca2++CO2↑+H2O
C.KHCO3与足量澄清石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2:Mn2++ClO-+H2O=MnO2↓+Cl-+2H+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:填空题
向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式__________________。
(2)下列三种情况下,离子方程式与(1)相同的是__________(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
若在A项所得溶液中,继续滴加Ba(OH)2溶液,此步反应的离子方程式为:________________

(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用右上图中的 曲线表示(填序号)。
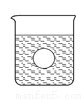
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com