
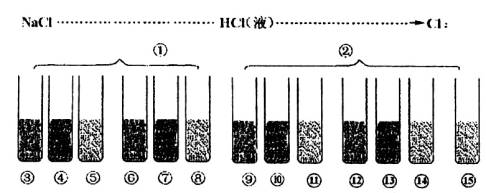
如下图所示,写出各步变化的化学方程式,并回答有关问题:
【注:①KCl ②MnO2 ③石蕊 ④Zn ⑤CuO ⑥Fe(OH)3 ⑦AgNO3 ⑧石灰石 ⑨石蕊 ⑩干红布条 11湿红布条 12H2S溶液 13NaI和CCl4 14KI淀粉
15NaOH溶液】
(1)反应方程式________________________体现浓硫酸的________性。
(2)反应方程式________________________体现浓盐酸的________性。
(3)现象______________________________体现盐酸的________性。
(4)现象________反应方程式________体现盐酸的________性,盐酸在反应中做________剂。
(5)现象________反应方程式________。
(6)现象________反应方程式________反应类型________是否氧化还原反应________。
(7)现象________反应方程式________常用于检验________离子。
(8)现象________反应方程式________此反应常用于制取________生成的气体,通入澄清石灰水现象________常用于检验________离子的存在。
(9)现象________说明氯气的水溶液是________性,且具有________性。
(10)现象________________________解释原因________________________________。
(11)现象________________________解释原因________________________________。
(12)现象________________________反应方程式________________,说明氯和硫比较________氧化性较强。
(13)现象_______________解释原因________________________。
(14)现象________________反应方程式________________解释原因________。
(15)现象________________反应方程式________实验室制氯气时,此反应常用于________。
(1)2KCl+H2SO4(浓)  
练习册系列答案
 激活思维优加课堂系列答案 激活思维优加课堂系列答案 活力试卷系列答案 活力试卷系列答案 课课优能力培优100分系列答案 课课优能力培优100分系列答案
相关习题
科目:高中化学 来源: 题型:阅读理解 Ⅰ.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答: (1)在一定体积的恒容密闭容器中,进行如下化学反应:N2(g)+3H2(g)  2NH3(g) 2NH3(g)其化学平衡常数K与温度t的关系如下表:
①比较K1、K2的大小:K1 > > K2(填“>”、“=”或“<”).②判断该反应达到化学平衡状态的依据是 AC AC (填序号).A.2v(H2)(正)=3v(NH3)(逆) B.v(N2)(正)=3v(H2)(逆) C.容器内压强保持不变 D.混合气体的密度保持不变 (2)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似. ①写出盐酸肼第一步水解反应的离子方程式 N2H62++H2O  [N2H5?H2O]++H+ [N2H5?H2O]++H+N2H62++H2O . [N2H5?H2O]++H+ [N2H5?H2O]++H+②盐酸肼水溶液中离子浓度的排列顺序正确的是 A A (填序号).A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-) B.c(Cl-)>c([N2H5?H2O+])>c(H+)>c(OH-) C.c(N2H62+)+c([N2H5?H2O+])+c(H+)=c(Cl-)+c(OH-) D.c(N2H62+)>c(Cl-)>c(H+)>c(OH-) Ⅱ.水体中重金属铅的污染问题备受关注.查资料得知Pb4+具有很强的氧化性.水中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2(在水中溶解度小)、Pb(OH)3-、Pb(OH)42-,各形态的物质的量的分数α随溶液pH变化的关系如下图所示: 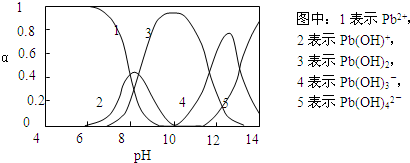 (1)Pb(NO3)2溶液中,c(Pb2+)/c(NO3-) < < 1/2(填“>”、“=”、“<”).(2)向Pb(NO3)2溶液滴加盐酸,溶液中c(Pb2+)/c(NO3-)没有变大,反而变小并有沉淀生成,则生成的沉淀可能为 PbCl2 PbCl2 .(3)向Pb(NO3)2溶液中滴加NaOH溶液,溶液也变浑浊,在pH约为 10 10 时生成沉淀最多,继续滴加NaOH溶液,混合体系又逐渐变澄清.pH=13时,混合体系中发生的主要反应的离子方程式为:Pb(OH)3-+OH-=Pb(OH)42- Pb(OH)3-+OH-=Pb(OH)42- .查看答案和解析>> 科目:高中化学 来源:物理教研室 题型:058 如下图所示,写出各步变化的化学方程式,并回答有关问题:
【注:①KCl ②MnO2 ③石蕊 ④Zn ⑤CuO ⑥Fe(OH)3 ⑦AgNO3 ⑧石灰石 ⑨石蕊 ⑩干红布条 11湿红布条 12H2S溶液 13NaI和CCl4 14KI淀粉 15NaOH溶液】
(1)反应方程式________________________体现浓硫酸的________性。 (2)反应方程式________________________体现浓盐酸的________性。 (3)现象______________________________体现盐酸的________性。 (4)现象________反应方程式________体现盐酸的________性,盐酸在反应中做________剂。 (5)现象________反应方程式________。 (6)现象________反应方程式________反应类型________是否氧化还原反应________。 (7)现象________反应方程式________常用于检验________离子。 (8)现象________反应方程式________此反应常用于制取________生成的气体,通入澄清石灰水现象________常用于检验________离子的存在。 (9)现象________说明氯气的水溶液是________性,且具有________性。 (10)现象________________________解释原因________________________________。 (11)现象________________________解释原因________________________________。 (12)现象________________________反应方程式________________,说明氯和硫比较________氧化性较强。 (13)现象_______________解释原因________________________。 (14)现象________________反应方程式________________解释原因________。 (15)现象________________反应方程式________实验室制氯气时,此反应常用于________。
查看答案和解析>> 科目:高中化学 来源:2013届吉林省汪清县第六中学高三第一次月考化学试卷(带解析) 题型:填空题 (10分)已知化合物A、D、E、G焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多。A~H各物质的变化关系如下图所示。 查看答案和解析>> 科目:高中化学 来源:2012-2013学年吉林省高三第一次月考化学试卷(解析版) 题型:填空题 (10分)已知化合物A、D、E、G焰色反应时,火焰均呈黄色,其中A可用作家庭食品添加剂,也可用以治疗胃酸过多。A~H各物质的变化关系如下图所示。
写出各步反应的化学方程式 反应① 反应② 反应③ 反应④ 反应⑤
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |