
| A.①②④⑥ | B.①③ | C.②④⑤⑥ | D.③⑤⑥ |
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源:不详 题型:填空题
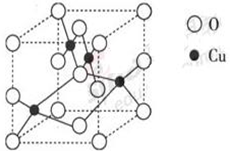
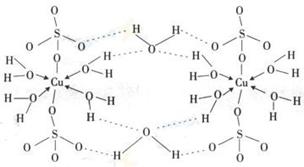
| A.在上述结构示意图中,所有氧原子都采用sp3杂化 |
| B.在上述结构示意图中,存在配位键、共价键和离子键 |
| C.胆矾是分子晶体,分子间存在氢键 |
| D.胆矾中的水在不同温度下会分步失去 |
 、④
、④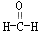 等,其中分子中C原子为SP2杂化的
等,其中分子中C原子为SP2杂化的查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溴、碘单质和CCl4中都含有卤素 |
| B.溴、碘是单质,CCl4是化合物 |
| C.Cl2、Br2、I2是非极性分子,CCl4也是非极性分子,而水为极性分子 |
| D.以上说法都不对 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
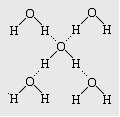
| A.除⑤⑥外 | B.除④⑦⑧外 | C.除④⑤⑥⑧外 | D.全对 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.O3在水中的溶解度和O2一样 | B.O3在水中的溶解度比O2小 |
| C.O3在水中的溶解度比O2要大 | D.没办法比较 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com