
| A. | 丁烷中碳、氢原子的个数比为4:10 | |
| B. | 丁烷中碳、氢两种元素的质量比是4:10 | |
| C. | 丁烷由碳、氢两种元素组成 | |
| D. | 一个丁烷分子由4个碳原子和10个氢原子构成 |
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 氨水呈碱性:NH3•H2O=NH4++OH- | |
| B. | 碳酸氢钠治疗胃酸过多:HCO3-+H+=CO2↑+H2O | |
| C. | 久置的浓硝酸呈黄色:4HNO3=4NO2↑+O2↑+2H2O | |
| D. | 久置碳酸氢铵有刺激性气味:NH4HCO3=NH3↑+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.02×1022个H2SO4分子在水中可电离生成2NA个H+ | |
| B. | 在0℃、101 kPa时,22.4 L氢气中含有NA个氢原子 | |
| C. | 14 g氮气中含有7NA个电子 | |
| D. | NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、H2SO4、H2SO3、H2S、S | B. | SO2、H2SO3、H2SO4、H2S、S | ||
| C. | SO2、H2SO3、H2SO4、SO3、S | D. | SO2、H2SO3、H2SO4、SO2、S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | NaBr、NaI、NaCl | C. | NaBr、NaI | D. | NaCl、I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
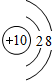 .
.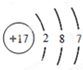 .
.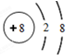
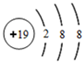 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | 氮化铝中N的化合价为-3价 | |
| C. | 因为具有抗冲击、导热性好等优良性能,所以氮化铝属于金属材料 | |
| D. | 合成氮化铝的反应符合“绿色化学”的思想 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com