
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如下图所示装置进行有关实验。
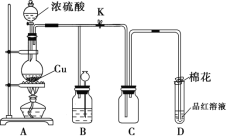
(1)装置A中发生反应的化学方程式为_________________________________________;
(2)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是________________,B中应放置的溶液是________(填字母);
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
(3)若装置C中盛有酸性KMnO4溶液,反应现象为_____________________,体现该气体的_____________(填“氧化性”或“还原性”);
(4)装置D中试管口放置的棉花应浸一种溶液,这种溶液是_____________,其作用是___________;
(5)实验中,取一定质量的铜片和一定体积18 mol·L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,其原因是________。
【答案】Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑ 广口瓶中液面下降,长颈漏斗液面上升 d 酸性高锰酸钾溶液褪色 还原性 NaOH溶液 吸收多余的SO2,防止污染空气 反应过程中浓硫酸被消耗,逐渐变稀,而铜不与稀硫酸反应
CuSO4+2H2O+SO2↑ 广口瓶中液面下降,长颈漏斗液面上升 d 酸性高锰酸钾溶液褪色 还原性 NaOH溶液 吸收多余的SO2,防止污染空气 反应过程中浓硫酸被消耗,逐渐变稀,而铜不与稀硫酸反应
【解析】
(1)装置A制备二氧化硫,据此书写方程式;
(2)根据装置B的作用是贮存多余的气体结合二氧化硫的性质分析解答;
(4)根据二氧化硫具有还原性,酸性高锰酸钾溶液具有氧化性分析;
(4)根据二氧化硫是大气污染物,需要进行尾气处理分析;
(5)根据浓硫酸和铜反应,稀硫酸不反应分析解答。
(1)浓硫酸具有强氧化性,在加热时可以氧化单质铜,生成硫酸铜、二氧化硫和水,则A装置中反应的方程式为:Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑;
CuSO4+2H2O+SO2↑;
(2)装置B的作用是贮存多余的气体,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,在密闭容器中随着气体的生成,广口瓶内压强增大,会使广口瓶内液面下降,长颈漏斗中液面上升,最终达到内外大气压相同,即实验现象是广口瓶中液面下降,长颈漏斗液面上升;二氧化硫气体是酸性氧化物,易溶于水,B中的试剂不能和二氧化硫发生反应,不能溶解二氧化硫,a.水能溶解二氧化硫不能储存气体,a错误;b.酸性KMnO4溶液能氧化二氧化硫为硫酸,不能储存气体,b错误;c.溴水能氧化二氧化硫不能储存气体,c错误;d.二氧化硫通入饱和NaHSO3溶液中,降低了二氧化硫的溶解度,不反应,可以用来储存气体,d正确;答案选d;
(3)二氧化硫具有还原性,酸性高锰酸钾溶液具有氧化性,因此若装置C中盛有酸性KMnO4溶液,二氧化硫被氧化,反应现象为酸性高锰酸钾溶液褪色,体现二氧化硫的还原性;
(4)二氧化硫气体排放到大气中污染环境,所以装置D中试管口放置的棉花中应浸一种液体能与二氧化硫反应,可以浸氢氧化钠溶液等碱性溶液,作用是吸收多余的二氧化硫气体,防止污染空气;
(5)一定质量的铜片和一定体积18molL-1的浓硫酸放在圆底烧瓶中共热,浓硫酸随着反应进行,浓度变小成为稀硫酸,稀硫酸不再和铜发生反应,所以有一定量的余酸剩余。


科目:高中化学 来源: 题型:
【题目】几种短周期元素的原子半径及主要化合价如下表,下列说法正确的是
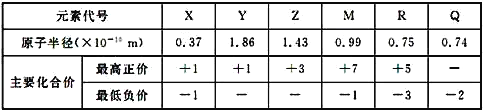
A. 离子半径:Y>Z>M
B. Y、Z、M三种元素的最高价氧化物的水化物两两之间会反应
C. 化合物XM、YM都是电解质.熔融状态下都能导电
D. 气态氢化物稳定性R>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列给出的几种氯化物的熔点和沸点:
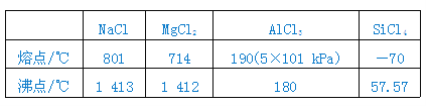
据表中所列数据判断下列叙述与表中相吻合的是( )
A. AlCl3在加热条件下能升华 B. SiCl4晶体属于原子晶体
C. AlCl3晶体是典型的离子晶体 D. NaCl的晶格能比MgCl2小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下图甲、乙、丙均为验证铜和浓硝酸反应的装置:

(1)甲、乙、丙三个装置中共同发生的化学方程式是___________________。
(2)和甲装置相比,乙装置的优点是
①________________________________________________,
②_______________________________________________。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。实验时先关闭活塞c,再打开活塞a、b,才能使NO2气体充满②试管;当气体充满②试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入②试管,应该如何操作_________________。
(4)②试管中的NO2和水充分反应后,所得溶液物质的量浓度的最大值是_____mol/L (气体体积按标准状况计算)。
II.证明卤族元素的非金属性强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性检查)

实验过程:Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。 Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是________________________________________。
(2)B中溶液发生反应的离子方程式是____________________________________。
(3)为验证溴的氧化性强于碘,过程 Ⅳ 的操作和现象是__________________。
(4)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,原子半径逐渐________,得电子能力逐渐________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 氯化铵受热固体消失和干冰升华只需克服分子间作用力
B. NaF、H2SO4中所含化学键类型相同
C. I2、Br2、Cl2、F2熔沸点逐渐升高
D. HCl气体溶于水和NaOH熔化破坏的化学键类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。已知断裂1 mol N—N键吸收193 kJ热量,断裂1 mol N≡N 键吸收941 kJ热量,则( )
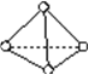
A. N4是一种新型化合物
B. 1 mol N4气体转化为N2时ΔH=+724 kJ/mol
C. N4是N2的同系物
D. 1 mol N4气体转化为N2时ΔH=-724 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的密闭容器中发生2SO2+O2 ![]() 2SO3反应,现控制下列三种不同的条件:①在400℃时,10molSO2与5molO2反应;②在400℃时,20molSO2与5molO2反应;③在300℃时,10molSO2与5molO2反应;
2SO3反应,现控制下列三种不同的条件:①在400℃时,10molSO2与5molO2反应;②在400℃时,20molSO2与5molO2反应;③在300℃时,10molSO2与5molO2反应;
(1)开始时正反应速率最快的是_________。
(2)若10min内测得第①组的平均反应速率为:V(SO2)=0.4mol/(L·min),则10min时,生成的SO3浓度为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
(1)查阅资料知:草酸晶体175℃分解成CO2、CO、H2O,请写出草酸晶体分解的化学反应方程式:_____。
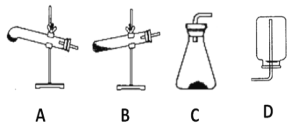
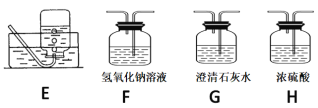
(2)请用下列的装置(图中加热装置已略去)分解草酸晶体以制备少量CO气体,最佳的连接顺序为:________。(填字母序号)
(3)设计实验证明草酸为弱酸的方案及其现象均正确的有_____________(填序号)。
A.室温下,测0.1mol/L的H2C2O4溶液与H2SO4溶液的pH,硫酸溶液的pH比草酸的小;
B.室温下,取pH=3的H2C2O4溶液稀释100倍后,测其pH<5;
C.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL。
(4)现需要配制900mL1mol/L的草酸溶液。
①需要的仪器有托盘天平(带砝码)、钥匙、烧杯、量筒、胶头滴管、_________、__________(填仪器名称)。
②下列操作会使所配溶液浓度偏低的是__________。(填字母)
A.称量时用了生锈的砝码
B.容量瓶未干燥即用来配制溶液
C.H2C2O4·2H2O晶体失去了部分结晶水
D.定容时,仰视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(5)用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数)。
①滴定过程中反应的离子方程式为_____________________________________________。
②量取KMnO4样品溶液应选用__________(填“酸式”或“碱式”)滴定管;若量取KMnO4样品溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将________(填“偏大”、“偏小”或“不变”)。
③现取KMnO4粗品10g,配成100mL溶液,取25.0 mL用(4)中配制的草酸溶液滴定,并进行3次平行实验,所用的草酸溶液的体积分别为23.00 mL、20.02 mL、19.98 mL,请问KMnO4粗品的质量分数为______________。(已知:KMnO4的摩尔质量为158g/mol)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com