
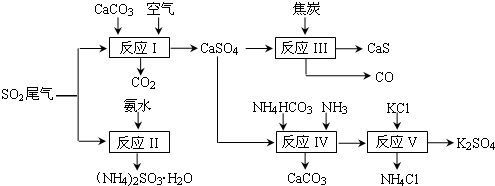
���� ��1�������ᰱ�е���Ϊ+4�ۣ��ױ������е�����������
��2��A����������ͼ��Ϸ�Ӧ����������������Ŀ����������������Ϊ����ƣ�
B����Ӧ��ѧ����ʽΪ��CaSO4+4C=CaS+4CO����
C����ֹ̼��������¶ȹ���ʱ�ֽ⣻
D���Ȼ����һ�ֵ��ʣ�
��� �⣺��1���Ա����Ӿ��л�ԭ�ԣ������е��������������ԣ������ᰱ��+4�۵�����л�ԭ�ԣ�
�ʴ�Ϊ����ֹ������隣�������
��2��A�������Ŀ����������������Ϊ����ƣ���A��ȷ��
B����Ӧ��ѧ����ʽΪ��CaSO4+4C=CaS+4CO������B��ȷ��
C����ֹ̼��������¶ȹ���ʱ�ֽ�ò�����Ҫ��Ŀ������C��ȷ��
D���Ȼ�狀�NԪ�أ���һ�ֵ��ʣ���D��ȷ��
�ʴ�Ϊ��ABCD��
���� ���⿼�������������ʼ����ʵ��Ʊ���Ϊ��Ƶ���㣬����ϰ���е���Ϣ�������ķ�ӦΪ���Ĺؼ�����Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���ӣ�0.1mol/L�� | Cu2+ | Fe2+ | Fe3+ | �ṩ��ҩƷ��������Ҫѡ��ʹ�ã� |
| �������↑ʼ����pH | 4.7 | 7.0 | 1.9 | Cl2��NaOH��Һ��CuO��Cu |
| �������������ȫpH | 6.7 | 9.0 | 3.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3-CH=CH2��  | |
| B�� |  �� ��  | |
| C�� | �ױ��Ͷ��ױ� | |
| D�� | CH2=CH-CH=CH2��CH3-CH2-CH2-C��CH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �Ӻ�ˮ�п���ȡʳ�� | |
| B�� | ��ˮ����ɵõ�ˮ | |
| C�� | ֱ�ӵ�⺣ˮ�ɵ�þ | |
| D�� | �Ӻ�ˮ�еõ���ˮ�ķ����������������������ӽ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| Mn��OH��2 | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | |
| ��ʼ����ʱ | 8.3 | 6.3 | 2.7 | 4.7 |
| ��ȫ����ʱ | 9.8 | 8.3 | 3.7 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 37% | B�� | 63% | C�� | 54% | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �Լ�M ��HBr������HBr��Ŀ���dz�ȥ������Ca��OH��2 | |
| B�� | ����IΪ���ˣ�����ΪFe��Fe��OH��2��Fe��OH��3��������Ϊ�ؽᾧ�������������Ϊ����Ũ������ȴ��Ʒ��ϴ�ӡ����� | |
| C�� | �Ƶõ�CaBr2•2H2O ����ͨ�����·����ⶨ���ȣ���ȡһ��������Ʒ����ˮ����������Na2CO3��Һ����ַ�Ӧ����ˣ�������ϴ�ӡ���ɡ���ȴ�������������ó�CaBr2•2H2O�Ĵ��� | |
| D�� | ��ҵ��Ҳ���Խ�����ͨ��ʯ���飬�������壬��65����з�Ӧ���Ƶ��廯�ƣ��˷�Ӧ�л�������һ����ɫ���壬�÷�Ӧ�Ļ�ѧ����ʽΪ3Ca��OH��2+3Br2+2NH3$\frac{\underline{\;\;��\;\;}}{\;}$3CaBr2+N2+6H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com