
分析 甲:NaOH溶液 $\stackrel{CO_{2}}{→}$Na2CO3溶液中,反应终点不易控制,易混有碳酸氢钠;
乙:NaOH溶液$→_{①}^{CO_{2}}$ NaHCO3溶液 $→_{②}^{加热蒸干、灼烧}$Na2CO3固体$\stackrel{H_{2}O}{→}$Na2CO3溶液,过程多,操作复杂;
丙:NaOH溶液 $→_{③}^{CO_{2}}$NaHCO3溶液$→_{①}^{NaOH溶液}$Na2CO3溶液,则两个反应中NaOH的量相同,即恰好发生NaOH+NaHCO3=Na2CO3+H2O,以此来解答.
解答 解:(1)由实验方案及物质的性质可知,甲方案的缺点为CO2的通入量不易控制;乙方案的缺点为过程烦琐,操作复杂,
故答案为:CO2的通入量不易控制;过程烦琐,操作复杂;
(2)由NaOH+NaHCO3=Na2CO3+H2O可知,采用丙方案制取纯Na2CO3溶液,其实验的关键是反应③应充分进行,反应③与④所用NaOH溶液的体积应相等,
故答案为:反应③应充分进行,③步骤后将NaHCO3溶液煮沸排除过量CO2,反应③④所用NaOH溶液的体积应相等;
(3)设混合物中碳酸钠、碳酸氢钠的质量分别为x、y,
若知道混合物的质量m,沉淀的总质量n,则
$\left\{\begin{array}{l}{x+y=m}\\{\frac{x}{106}+\frac{y}{84}=\frac{n}{100}}\end{array}\right.$,
则解二元一次方程可计算含量,
故答案为:能;固体样品的质量和沉淀的总质量.
点评 本题考查碳酸钠、碳酸氢钠的性质实验,为高频考点,把握性质及发生的反应、混合物计算为解答的关键,侧重分析与实验能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Mg2+、Fe3+、NO3-、SCN- | B. | Al3+、Fe2+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、HCO3- | D. | Na+、CH3COO-、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
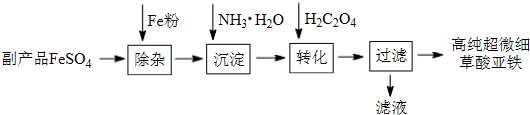
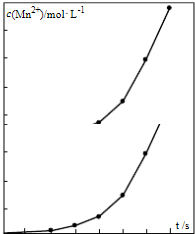
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.3gNa投入到97.7g水中形成的溶液溶质质量分数为4% | |
| B. | 25gCuSO4•5H2O溶于75g水之后,溶质的质量分数为16% | |
| C. | 相同质量的Na2O和Na2O2溶于相同体积的足量水中,所得溶液的质量分数相同 | |
| D. | 向含Na2CO310.6g的饱和碳酸钠溶液中通入过量CO2,所得溶液溶质质量为16.8g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫代硫酸钠溶液与稀硫酸混合:S2O32-+2H+═S↓+SO2↑+H2O | |
| B. | 向CuSO4溶液中通入H2S气体:Cu2++S2-═CuS↓ | |
| C. | 向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-═Ag2S↓+2Cl- | |
| D. | 重铬酸钾的溶液中存在着如下平衡:Cr2O72-(橙红色)+H2O═2H++2CrO42-(黄色) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
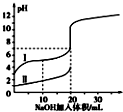 室温下,用 0.100mol/L NaOH 溶液分别与 20.00mL 0.100mol/L 的盐酸和醋酸反应,pH 与滴入碱的体积关系如图所示. 已知醋酸电离常数 K=1.7×10 -5下列说法正确的是( )
室温下,用 0.100mol/L NaOH 溶液分别与 20.00mL 0.100mol/L 的盐酸和醋酸反应,pH 与滴入碱的体积关系如图所示. 已知醋酸电离常数 K=1.7×10 -5下列说法正确的是( )| A. | Ⅰ、Ⅱ分别表示盐酸和醋酸的反应曲线 | |
| B. | pH=7 时,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=170 | |
| C. | V(NaOH)=10.00 mL 时,醋酸溶液的导电性更强 | |
| D. | 向盐酸中加 NaOH 至 pH=12 时,V(NaOH)=200/9 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
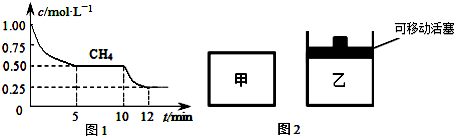
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂的作用 | B. | 还原剂的作用 | C. | 催化剂的作用 | D. | 吸附剂的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A气体是NH3,B气体是CO2 | |
| B. | 侯氏制碱法的工艺过程应用了物质溶解度的差异 | |
| C. | 第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 | |
| D. | 第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com