
分析 (1)根据n=$\frac{V}{Vm}$计算HCl的物质的量,根据m=nM计算HCl的质量,根据m=ρV计算水的质量,进而计算溶液的体积,根据c=$\frac{n}{V}$计算所得盐酸的物质的量浓度;
(2)计算碳酸钠的物质的量,依据方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑计算解答;
解答 解:(1)224LHCl的物质的量为$\frac{224L}{22.4L/mol}$=10mol,HCl的质量为10mol×36.5g/mol=365g,
635mL水的质量为635mL×1g/mL=635g,故溶液的质量为:635g+365g=1000g,
故所得盐酸的体积=$\frac{1000g}{1200g/L}$=$\frac{5}{6}$L,所得盐酸的物质的量浓度为:c=$\frac{10mol}{\frac{5}{6}L}$=12mol/L,
故答案为:12 mol/L;
(2)53g的Na2CO3物质的量$\frac{53g}{106g/mol}$=0.5mol;
依据:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
1 2 1
0.5mol n(HCl) n(CO2)
所以生成标况下二氧化碳体积为0.5mol×22.4L/mol=11.2L;
反应中消耗盐酸物质的量为0.5mol×2=1mol,消耗盐酸体积:$\frac{1mol}{12mol/L}$=0.0833L,即83.3mL;
故答案为:11.2L 83.3 mL.
点评 本题考查了物质的量计算,明确以物质的量为核心计算公式是解题关键,题目难度不大.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:选择题
 如图是部分短周期元素的原子序数与其某种常 见化合价的关系图,若用原子序数代表所对应的元素,则下列说法中不正确的有( )
如图是部分短周期元素的原子序数与其某种常 见化合价的关系图,若用原子序数代表所对应的元素,则下列说法中不正确的有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| t/min | 0 | 20 | 40 | 60 | 80 | 120 | |
| 第一次试验 | x(HI) | 1 | 0.90 | 0.85 | 0.815 | 0.795 | 0.784 |
| 第二次试验 | x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol Mg与足量盐酸反应生成氢气的体积为11.2升 | |
| B. | 标准状况下,11.2L SO2所含的原子数为1.5NA | |
| C. | 8gCH4所含的氢原子数为0.5NA | |
| D. | 46g NO2和N2O4的混合物所含的分子数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
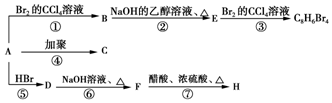
 .
. ,D
,D ,E
,E ,H
,H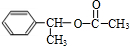 .
. +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaBr.
+NaBr.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 常温常压下,44g CO2含有的原子数为3NA | |
| C. | 常温常压下,11.2L氧气所含的原子数为NA | |
| D. | 标准状况下,11.2L H2O 含有的分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com