
 据报道,苹果醋是由苹果发酵而成的酸性饮品,其中的酸性物质主要是苹果酸.有关苹果酸的结构确定及合成过程如下:
据报道,苹果醋是由苹果发酵而成的酸性饮品,其中的酸性物质主要是苹果酸.有关苹果酸的结构确定及合成过程如下: .
.

 +n HO-CH2CH2-OH$\stackrel{一定条件}{→}$
+n HO-CH2CH2-OH$\stackrel{一定条件}{→}$ +(2n-1)H2O.
+(2n-1)H2O. 、
、 .
. 分析 Ⅰ氧的质量分数为59.7%,1mol该酸与足量的NaHCO3反应放出44.8L CO2,说明分子中含有2个-COOH,与足量的Na反应放出33.6L H2,为1.5mol,说明分子中含有3个-OH(包括-COOH)则至少含有5个O原子,如含有5个O,则相对原子质量为$\frac{5×16}{0.597}$=134,其相对分子质量大于112小于160,符合题意,核磁共振氢谱显示苹果酸中存在5种不同环境的H原子,则结构应为
Ⅱ75%(体积分数)的A水溶液常用于医疗消毒,A为CH3CH2OH,A连续发生氧化反应生成C,则B为CH3CHO,C为CH3COOH,由反应信息①可知,羧基连接的碳原子上的氢原子被溴原子取代,故D为Br-CH2-COOH,D发生水解反应生成E为HO-CH2-COONa,E酸化得到F为HO-CH2-COOH,F发生氧化反应得到G为HOOC-CHO,G与乙醛发生信息②中醛的加成反应生成H为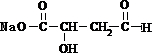 ,H酸化得到I为
,H酸化得到I为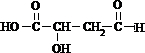 ,I发生氧化反应得到J为
,I发生氧化反应得到J为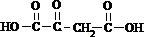 ,J与氢气发生加成反应得到苹果酸,以此解答该题.
,J与氢气发生加成反应得到苹果酸,以此解答该题.
解答 解:Ⅰ氧的质量分数为59.7%,1mol该酸与足量的NaHCO3反应放出44.8L CO2,说明分子中含有2个-COOH,与足量的Na反应放出33.6L H2,为1.5mol,说明分子中含有3个-OH(包括-COOH)则至少含有5个O原子,如含有5个O,则相对原子质量为$\frac{5×16}{0.597}$=134,其相对分子质量大于112小于160,符合题意,核磁共振氢谱显示苹果酸中存在5种不同环境的H原子,则结构应为
1.根据上面的分析可知,苹果酸中的氧原子个数为5,苹果酸结构为
故答案为:5;C4H6O5;
2.(1)根据上面的分析可知,一个苹果酸分子中有1个-OH,
故答案为:1;
(2)根据上面的分析可知,苹果酸的结构简式为
故答案为:
Ⅱ75%(体积分数)的A水溶液常用于医疗消毒,A为CH3CH2OH,A连续发生氧化反应生成C,则B为CH3CHO,C为CH3COOH,由反应信息①可知,羧基连接的碳原子上的氢原子被溴原子取代,故D为Br-CH2-COOH,D发生水解反应生成E为HO-CH2-COONa,E酸化得到F为HO-CH2-COOH,F发生氧化反应得到G为HOOC-CHO,G与乙醛发生信息②中醛的加成反应生成H为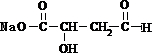 ,H酸化得到I为
,H酸化得到I为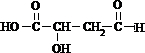 ,I发生氧化反应得到J为
,I发生氧化反应得到J为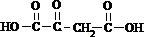 ,J与氢气发生加成反应得到苹果酸,
,J与氢气发生加成反应得到苹果酸,
(1)D→E反应的化学方程式为:Br-CH2-COOH+2NaOH$→_{△}^{水}$HO-CH2-COONa+NaBr+H2O,
故答案为:Br-CH2-COOH+2NaOH$→_{△}^{水}$HO-CH2-COONa+NaBr+H2O;
(2)上述合成线路中,涉及到的加成反应的有EG的反应以及J生成苹果酸的反应,共2步,
故答案为:2;
(3)苹果酸消去一分子水后的产物为


故答案为:n

(4)与苹果酸含有相同种类和数目的官能团的同分异构体的结构简式为:

故答案为:

点评 本题考查有机物的推断,注意计算确定苹果酸的分子式,结合含有的官能团及H原子种类判断苹果酸的结构简式,也可以利用乙烯发生的系列反应进行推断,是对有机化学的综合可知,难度中等.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:解答题

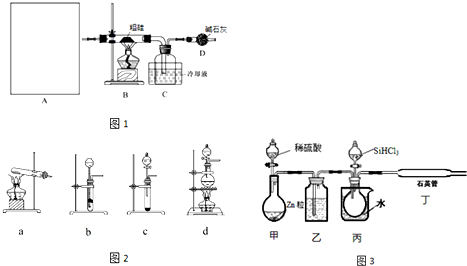
| 物质 | SiCl4 | SiHCl3 | AlCl3 | FeCl3 |
| 沸点/℃ | 57.7 | 33.0 | - | 315 |
| 升华温度/℃ | - | - | 180 | 300 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 25 | t1 | t2 |
| Kw/mol2•L-2 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素强 | |
| B. | 发生氧化还原反应时,A原子失去的电子比B原子多,证明A的金属性一定比B强 | |
| C. | 适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2=2FeCl3+4FeI3 | |
| D. | 一定量氯气通入30 mL 10.00 mol•L-1的氢氧化钠溶液中,加热后形成NaCl、NaClO、NaClO3共存的溶液,若反应中转移的电子为n mol,则0.15<n<0.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 Ⅰ.A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示. 若A、B、C的焰色反应均呈黄色,水溶液均为碱性.
Ⅰ.A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示. 若A、B、C的焰色反应均呈黄色,水溶液均为碱性.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3与水反应生成NH3•H2O | B. | NH3与水分子之间形成氢键 | ||
| C. | NH3和水分子的相对分子质量接近 | D. | NH3是极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖和维生素C中含有的碳、氧原子个数相等 | |
| B. | 葡萄糖和维生素C中碳元素和氧元素的质量比都是l:1 | |
| C. | -个葡萄糖分子比-个维生素C分子多4个氢原子 | |
| D. | -个维生素C分子中的中子数和电子数一定相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com