
| A. | ①③⑥ | B. | ①②④ | C. | ②④⑤ | D. | ③④⑤ |
分析 离子化合物一定存在离子键,可能存在共价键,共价化合物中只存在共价键,以共价键结合的物质可能为原子晶体,也可能为分子晶体,在分子晶体中还存在分子间作用力,据此解答.
解答 解:①NaOH是离子化合物,钠离子与氢氧根离子之间存在离子键,氧原子与氢原子之间存在共价键,故选;
②SiO2是共价化合物,只存在共价键,故不选;
③NH4Cl是离子化合物,铵根离子与氯离子直接存在离子键,氮原子与氢原子之间存在共价键,故选;
④金刚石是原子晶体,只有共价键,故不选;
⑤NaCl是离子化合物,只存在离子键,故不选; ⑥白磷存在P-P共价键,属于分子晶体,分子间通过分之间作用力结合,故选;
故选:A.
点评 本题考查化学键和晶体,注意化学键的形成规律及分子晶体中存在分子间作用力即可解答,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、K+、Cl-、SO32- | B. | NH4+、Fe2+、I-、SO42- | ||
| C. | Na+、K+、ClO-、S2- | D. | Na+、S2O32-、AlO2-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水与足量的 FeBr2溶液反应:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- | |
| B. | NaHCO3溶液与 NaOH溶液反应:HCO3-+OH-=CO32-+H2O | |
| C. | NaHCO3溶液与盐酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | NaHCO3溶液与CaCl2;溶液反应:CO32-+Ca2+=CaCO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
. +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
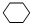 ,名称是环己烷,该烃的二氯代物有4种.
,名称是环己烷,该烃的二氯代物有4种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3?Fe3++3OH- | B. | NaHCO3?Na++HCO3- | ||
| C. | KClO3═K++Cl-+3O2- | D. | H2S?2H++S2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com