
某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、SO32-、HCO3-、Na+、Mg2+、Fe3+,所含离子的物质的量浓度均相同。为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如下实验:
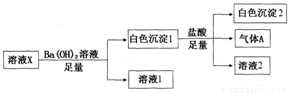
下列说法正确的是
A. 气体A可能是CO2或SO2
B. 溶液X中一定存在SO42-、HCO3-、Na+、Mg2+
C. 溶液X中一定不存在Fe3+和Mg2+,可能存在Na+
D. 分别在溶液1和溶液2中加入硝酸酸化的硝酸银溶液都能生成白色沉淀
科目:高中化学 来源:2016-2017学年湖南省株洲市高一下学期第一次月考化学试卷(解析版) 题型:简答题
实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
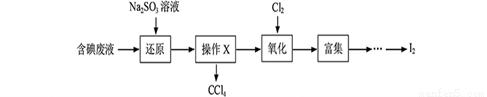
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为________________;该操作将I2还原为I-的目的是_____________________。
(2)操作X的名称为____________。
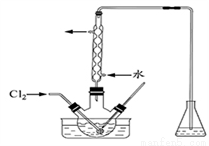
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在400C左右反应(实验装置如下图所示)。实验控制在较低温度下进行的原因是________________;锥形瓶里盛放的溶液为______________。
(4)已知:5SO32—+2IO3—+2H+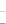 I2+5SO42—+H2O
I2+5SO42—+H2O
某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO3—中的一种或两种。请补充完整检验含碘废水中是否含有IO3—的实验方案(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在;_____________________________________________________________
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三第五次模拟考试理综化学试卷(解析版) 题型:简答题
研究含氮污染物的治理是环保的一项重要工作。合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ•mol﹣1
2C(s)+O2(g)=2CO(g) △H=﹣221.0kJ•mol﹣1
C(s)+O2(g)=CO2(g) △H=﹣393. 5kJ•mol﹣1
则汽车尾气处理的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=_____ kJ•mol﹣1,利于
该反应自发进行的条件是_______(选填“高温”或“低温”)。

(2)将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中发生反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g),反应过程中 部分物质的浓度变化如图所示:
反应从开始到9min时,用CO2表示该反应的速率是____________________(保留2位有效数字)
②第12min时改变的条件是______________(填“升温或降温”).
③第18min时建立新的平衡,此温度下的平衡常数为______________(列计算式),第24min时,若保持温度不变,再向容器中充入CO和N2各0.060mol,平衡将_____移动(填“正向”、“逆向”或“不”)。
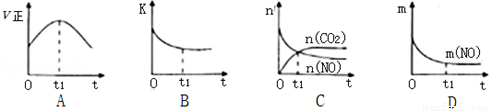
(3)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在t1时刻达到平衡状态的是________________(填序号)。
(如图中v正、K、n、m分别表示正反应速率、平衡常数、物质的量和质量)
(4)以氨为燃料可以设计制造氨燃料电池,产物无污染。若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为______________________________
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省抚顺市高三3月模拟考试理科综合化学试卷(解析版) 题型:选择题
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是
A. 同周期元素中X的金属性最强
B. 原子半径X>Y,离子半径X+>Z2-
C. 同族元素中Z的氢化物稳定性最高
D. 同周期元素中Y的最高价含氧酸的酸性最强
查看答案和解析>>
科目:高中化学 来源:2017届浙江省宁波市高三新高考选考适应性考试化学试卷(解析版) 题型:简答题
氯化铵、甲醇、氧化铝都是重要化合物。
(1)已知:
I NH4Cl(s)=NH3(g)+HCl(g) △H=+l63.9 kJ·mol-1
II HCl(g)+CH3OH(g) CH3Cl(g)+H2O(g) △H=-31.9kJ·mol-1
CH3Cl(g)+H2O(g) △H=-31.9kJ·mol-1
III NH4Cl(s)+CH3OH(g) NH3(g)+CH3Cl(g)+H2O(g)
NH3(g)+CH3Cl(g)+H2O(g)
① 反应III在_________条件下能自发反应(填“较高温度”、“较低温度”或“任何温度”),理由是_______________。
② 图1是反应III使用三种不同催化剂时得到的CH3Cl产率与温度关系的变化图。
己知:催化剂用量、催化剂粒数、n(甲醇):n(氯化铵)的值、甲醇进料速度、反应时间等测试条件都相同。
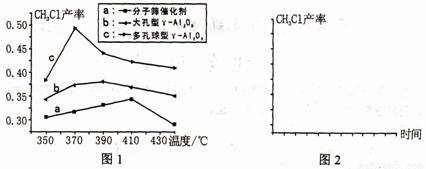
图1 中a曲线CH3Cl产率先增大后减小的原因是___________。请在图2中画出其它条件都相同时,在370 ℃下使用三种不同催化剂至反应平衡时,CH3Cl的产率与时间关系的变化曲线,并用a、b、c标出对应的曲线。_______________
(2)25 ℃时,在某浓度的NH4Cl溶液中滴加一定量的氨水至中性,此时测得溶液中c(Cl-)= 0.36mol · L-1,则混合溶液中c (NH3 · H2O)=_______mol · L-1。(25℃时,NH3·H2O的Kb=1.8×10-5)
(3)多孔Al2O3薄膜可作为催化剂载体、模板合成纳米材料等用途。现以高纯铝片作为阳极,不锈钢作为阴极,一定溶度的磷酸溶液作为电解质进行电解,即可初步制取多孔Al2O3膜。请写出该制取过程的阳极电极反应:__________________。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省宁波市高三新高考选考适应性考试化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A. 氯化钠熔化时离子键被破坏
B. 二氧化硅融化和干冰气化所破坏的作用力不相同
C. H2SO4、CCl4、NH3均属于共价化合物
D. HBr比HCl的热稳定性差说明HBr的分子间作用力比HCl弱
查看答案和解析>>
科目:高中化学 来源:2017届浙江省宁波市高三新高考选考适应性考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A. Zn与稀H2SO4反应:2Zn+2H+=2Zn2++H2↑
B. 氯气和水反应:Cl2+H2O=2H++Cl-+ClO-
C. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
D. 硫酸氢钠溶液与过量氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省大庆市高三第二次教学质量检测(二模)理科综合化学试卷(解析版) 题型:简答题
以铬铁矿为原料制备铬酸钾(K2Cr2O7)的工艺流程如下图所示。铬铁矿的主要成分可表示为FeO-Cr2O3和杂质SiO2。
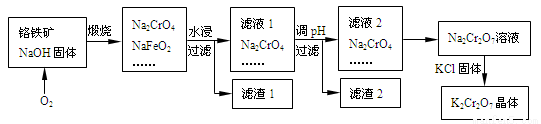
已知:①NaFeO2遇水强烈水解
②2CrO42-+2H+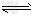 Cr2O72-+H2O
Cr2O72-+H2O
回答下列问题:
(1)K2CrO4中Cr元素的化合价是________。
(2)完成并配平煅烧铬铁矿生成Na2CrO4和NaFeO2的化学反应方程式________
FeO-Cr2O3+ O2+ NaOH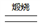 Na2CrO4+NaFeO2+ ;
Na2CrO4+NaFeO2+ ;
该反应的氧化产物是________。
(3)生成滤渣1中红褐色物质的化学反应方程式是____________。滤渣2的成分(填化学式)_______。
(4)滤液2存在平衡:2CrO42-(黄色)+2H+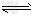 Cr2O72-(橙色)+H2O。若改变条件使上述平衡向正方向移动,则下列说法正确的是______。
Cr2O72-(橙色)+H2O。若改变条件使上述平衡向正方向移动,则下列说法正确的是______。
A.达到新平衡后,溶液PH一定增大
B.再达到新平衡前,正反应速率一定大于逆反应速率
C.该反应平衡常数可以不改变
D.达新平衡后,CrO42-的消耗速率等于Cr2O72-的消耗速率
(5)含铬废水中含有一定量的Cr2O72-和CrO42-,它们会对人体及生态系统产生很大的危害,必须进行处理。还原沉淀法是常用的一种方法:
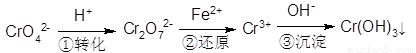
①上述流程中还原过程的离子反应方程式为:_______________。
②最终生成的Cr(OH)3在溶液中存在沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH—(aq)常温下,Cr(OH)3的Ksp=1×10-32,当c(Cr3+)降至1×10-3·mol·L-1,溶液的pH应调至4时______(填“有”或“没有”)沉淀生成。
Cr3+(aq)+3OH—(aq)常温下,Cr(OH)3的Ksp=1×10-32,当c(Cr3+)降至1×10-3·mol·L-1,溶液的pH应调至4时______(填“有”或“没有”)沉淀生成。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高一下学期第一次联考(3月)化学试卷(解析版) 题型:选择题
下列反应中,不属于HNO3类别通性的是( )
A. 4HNO3(浓)+S SO2↑+4NO2↑+2H2O B. HNO3+NaOH=NaNO3+H2O
SO2↑+4NO2↑+2H2O B. HNO3+NaOH=NaNO3+H2O
C. 2HNO3+CuO=Cu(NO3)2+H2O D. 2HNO3+CaCO3=Ca(NO3)2+CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com