
·ÖĪö £Ø1£©Ę½ŗā³£ŹżµČÓŚÉś³ÉĪļµÄÅضČĆŻÖ®»ż³żŅŌ·“Ó¦ĪļµÄÅضČĆŻÖ®»ż£¬×¢ŅāCĪŖ¹ĢĢ壻
£Ø2£©ÉżøßĪĀ¶Č£¬Ę½ŗā³£ŹżŌö“ó£¬ĖµĆ÷Ę½ŗāÕżĻņŅĘ¶Æ£»
£Ø3£©“ļµ½Ę½ŗāŹ±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ø÷ĪļÖŹµÄÅØ¶Č²»±ä£¬ŅŌ“ĖŃÜÉśµÄĪļĄķĮæ²»±ä£¬ŅŌ“ĖÅŠ¶Ļ£»
£Ø4£©ŌŚ1 000”ęĻĀ£¬Ä³Ź±æĢCOµÄĪļÖŹµÄĮæĪŖ1.0mol£¬“ĖŹ±K=1£¬¼ĘĖćø÷ĪļÖŹµÄĮæÅضČĆŻ£¬ÓėKĻą±Č½Ļ£¬æÉÅŠ¶ĻŹĒ·ń“ļµ½Ę½ŗāדĢ¬£¬²¢¼ĘĖć×Ŗ»ÆĀŹ£®
½ā“š ½ā£ŗ£Ø1£©CĪŖ¹ĢĢ壬K=$\frac{c£ØCO£©c£Ø{H}_{2}£©}{c£Ø{H}_{2}O£©}$£¬¹Ź“š°øĪŖ£ŗK=$\frac{c£ØCO£©c£Ø{H}_{2}£©}{c£Ø{H}_{2}O£©}$£»
£Ø2£©ÉżøßĪĀ¶Č£¬Ę½ŗā³£ŹżŌö“ó£¬ĖµĆ÷Ę½ŗāÕżĻņŅĘ¶Æ£¬Ōņ·“Ó¦ĪŖĪüČČ·“Ó¦”÷H£¾0£¬¹Ź“š°øĪŖ£ŗ£¾0£»
£Ø3£©A”¢Ģ¼ĪŖ¹ĢĢå£¬ČŻĘ÷ÖŠĘųĢåµÄĆÜ¶Č²»±ä£¬æÉĖµĆ÷“ļµ½Ę½ŗāדĢ¬£¬¹ŹAÕżČ·£»
B”¢Éś³Éa mol COµÄĶ¬Ź±ĻūŗÄa mol H2£¬ĖµĆ÷ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬æÉĖµĆ÷“ļµ½Ę½ŗāדĢ¬£¬¹ŹBÕżČ·£»
C”¢c£ØH2O£©=c£ØCO£©£¬²»ÄÜĖµĆ÷ÅØ¶Č²»±ä£¬²»ÄÜĖµĆ÷“ļµ½Ę½ŗāדĢ¬£¬¹ŹC“ķĪó£»
D”¢»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»±ä£¬æÉĖµĆ÷ĘųĢåµÄÖŹĮæ²»±ä£¬ĖµĆ÷“ļµ½Ę½ŗāדĢ¬£¬¹ŹDÕżČ·£®
¹Ź“š°øĪŖ£ŗABD£»
£Ø4£©ŌŚ1 000”ęĻĀ£¬Ä³Ź±æĢCOµÄĪļÖŹµÄĮæĪŖ1.0mol£¬Ōņ
C£Øs£©+H2O£Øg£©?CO£Øg£©+H2£Øg£©
ĘšŹ¼£Ømol/L£© 2 0 0
×Ŗ»Æ£Ømol/L£© 1 1 1
Ę½ŗā£Ømol/L£© 1 1 1
$\frac{1”Į1}{1}$=1£¬ĖµĆ÷“ļµ½Ę½ŗāדĢ¬£¬
ŌņvÕż=vÄę£¬
“ĖŹ±H2O£Øg£©µÄ×Ŗ»ÆĀŹĪŖ$\frac{1}{2}”Į100%$=50%£¬
¹Ź“š°øĪŖ£ŗ=£»50%£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆŃ§Ę½ŗāµÄÓŠ¹Ų¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦µÄ漲飬ÄŃ¶Č²»“ó£¬Ć÷Č·”°Čż¶ĪŹ½”±·ØŹĒ»ÆŃ§Ę½ŗā¼ĘĖć³£ÓĆµÄ½āĢā·½·Ø£¬Ó¦ŹģĮ·ÕĘĪÕ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ź³“׳żĖ®¹ø | B£® | Ź³ĪļøÆĄĆ | ||
| C£® | ŌŚøßĪĀĻĀÓĆš¤ĶĮÉÕÖĘĢÕ“É | D£® | ·ÖŅŗ·Ø·ÖĄėĖÄĀČ»ÆĢ¼ÓėĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
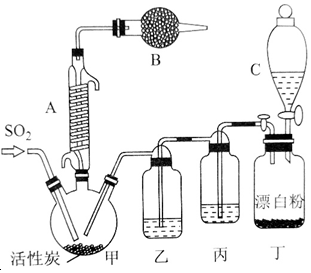 ÓŠ¹ŲŠÅĻ¢ČēĻĀ£ŗĮņõ£ĀČĶس£Ģõ¼žĻĀĪŖĪŽÉ«ŅŗĢ壬ČŪµćĪŖ-54.1”ę£¬·ŠµćĪŖ69.1”ę£¬ŌŚ³±ŹŖæÕĘųÖŠ”°·¢ŃĢ”±£»100”ęŅŌÉĻæŖŹ¼·Ö½ā£¬Éś³É¶žŃõ»ÆĮņŗĶĀČĘų£¬³¤ĘŚ·ÅÖĆŅ²»į·¢Éś·Ö½ā£®»Ų“šĻĀĮŠĪŹĢā£ŗ
ÓŠ¹ŲŠÅĻ¢ČēĻĀ£ŗĮņõ£ĀČĶس£Ģõ¼žĻĀĪŖĪŽÉ«ŅŗĢ壬ČŪµćĪŖ-54.1”ę£¬·ŠµćĪŖ69.1”ę£¬ŌŚ³±ŹŖæÕĘųÖŠ”°·¢ŃĢ”±£»100”ęŅŌÉĻæŖŹ¼·Ö½ā£¬Éś³É¶žŃõ»ÆĮņŗĶĀČĘų£¬³¤ĘŚ·ÅÖĆŅ²»į·¢Éś·Ö½ā£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
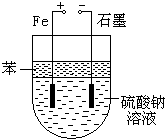 ŹµŃéŹŅÓĆNaOHŗĶFeSO4ÖĘČ”Fe£ØOH£©2Ź±£¬Fe£ØOH£©2ŗÜČŻŅ×±»Ńõ»Æ£¬Čō²ÉÓĆČēĶ¼ĖłŹ¾×°ÖĆÖĘČ”£¬æÉŅŌµĆµ½½Ļ“æ¾»µÄFe£ØOH£©2£®
ŹµŃéŹŅÓĆNaOHŗĶFeSO4ÖĘČ”Fe£ØOH£©2Ź±£¬Fe£ØOH£©2ŗÜČŻŅ×±»Ńõ»Æ£¬Čō²ÉÓĆČēĶ¼ĖłŹ¾×°ÖĆÖĘČ”£¬æÉŅŌµĆµ½½Ļ“æ¾»µÄFe£ØOH£©2£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
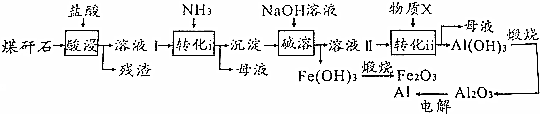
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe3O4ŹĒ»¹Ō¼Į | B£® | COŹĒŃõ»Æ¼Į | ||
| C£® | 1mol Fe3O4µĆµ½6molµē×Ó | D£® | 4molCOŹ§Č„8molµē×Ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com