
分析 在所得溶液中滴入AgNO3溶液,生成白色沉淀,可能生成AgCl或Ag2CO3,再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成,说明两种沉淀都含有,一定含有KCl、K2CO3,不能确定是否含有KNO3,以此解答该题.
解答 解:在所得溶液中滴入AgNO3溶液,生成白色沉淀,可能生成AgCl或Ag2CO3,再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成,说明两种沉淀都含有,一定含有KCl、K2CO3,不能确定是否含有KNO3,
(1)由以上分析可知一定含有KCl、K2CO3,不能确定是否含有KNO3,故答案为:KCl、K2CO3;KNO3;
(2)碳酸银可溶于硝酸,生成硝酸银和二氧化碳气体,反应的离子方程式为Ag2CO3+2H+=2Ag++CO2↑+H2O,故答案为:Ag2CO3+2H+=2Ag++CO2↑+H2O.
点评 本题考查物质的检验和鉴别,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质,解答本题要从物质的颜色、物质之间相互作用时的实验现象等方面进行分析、判断,从而得出正确的结论,难度不大.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | SiO2、CO2 都是酸性氧化物,都能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应的产物相同 | |
| C. | SO2、NO、CO2都是大气污染物,在空气中都能稳定存在 | |
| D. | HCl、HNO3都是强酸,和FeO的反应都属于复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度实验次数 | 起始温度t2 /℃ | 终止温度 t2 /℃ | 温度差平均值 (t2- t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 25.0 | 25.2 | 25.1 | 28.5 | 3.4 |
| 2 | 24.9 | 25.1 | 25.0 | 28.3 | 3.3 |
| 3 | 25.6 | 25.4 | 25.5 | 29.0 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有Cl2 | B. | 一定有SO2 和NO | ||
| C. | 可能有NO2 | D. | 一定有SO2,可能有NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
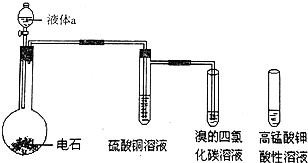 如图是实验室制取乙炔气体及乙炔的性质实验的装置,气密性已检验,部分夹持装置略.
如图是实验室制取乙炔气体及乙炔的性质实验的装置,气密性已检验,部分夹持装置略. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
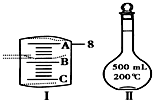 实验室要用NaCl晶体配制500mL 0.2mol•L-1NaCl溶液,回答下列问题:
实验室要用NaCl晶体配制500mL 0.2mol•L-1NaCl溶液,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可吸入颗粒物中含有的铅?镉?铬?钒?砷等对人体有害的元素均为金属元素 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广乙醇?汽油的使用 | |
| C. | 单质硅晶体是将太阳能转化为电能的常用材料 | |
| D. | 新型能源生物柴油和矿物油的主要化学成分相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com