


科目:高中化学 来源: 题型:
| A、分子晶体中一定存在分子间作用力,不一定存在共价键 |
| B、H2O沸点高于NH3,是因为H2O分子间存在氢键而NH3分子间不存在氢键 |
| C、含有金属离子的晶体一定是离子晶体 |
| D、二氧化硅的结构式:Si=O=Si |
查看答案和解析>>
科目:高中化学 来源: 题型:

| n(CH3OH) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、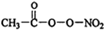 (PAN)等二次污染物.
(PAN)等二次污染物.| m |
| n |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | B-H | B-O | B-B |
| 键能(kJ?mol-1) | 389 | 561 | 293 |

查看答案和解析>>
科目:高中化学 来源: 题型:
 如图Ⅰ、Ⅱ、Ⅲ所示装置进行有关实验,将A逐滴加入B中.
如图Ⅰ、Ⅱ、Ⅲ所示装置进行有关实验,将A逐滴加入B中.| 浓硫酸 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ;②
;② ;③
;③ .则下列有关这三种原子的叙述中正确的是( )
.则下列有关这三种原子的叙述中正确的是( )| A、属于不同的元素 |
| B、具有相同的质量数 |
| C、具有不同的核电荷数 |
| D、化学性质相似 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com