
下列关于常温下,pH=3的醋酸溶液(I)和 pH=11的氢氧化钠溶液(Ⅱ)的说法正确的是( )
A.I和Ⅱ的物质的量浓度均为0.001mol·L-1
B.将I稀释10倍,溶液中 c(CH3COOH)、 c(OHˉ)均减小
C.I和Ⅱ溶液混合,若c(OH-)>c(H+),则氢氧化钠过量
D.I和Ⅱ等体积混合后,溶液中离子浓度大小为c(CH3COO-)>c(Na+)> c(H+)> c(OH--)
科目:高中化学 来源: 题型:
(1)____S+____KOH===____K2S+____K2SO3+____H2O
(2)____P4+____KOH+____H2O===____K3PO4+____PH3
查看答案和解析>>
科目:高中化学 来源: 题型:
上海人张霞昌在芬兰发明了“纸电池”,这种一面镀锌、一面镀二氧化锰的超薄电池在使用印刷与压层技术后,变成一张可任意裁剪大小的“电纸”,纸内的离子“流过”水和氧化锌组成的电解质溶液,电池总反应式为:
Zn+2MnO2+H2O===ZnO+2MnOOH。下列说法正确的是
A.该电池的正极材料为锌
B.该电池反应中二氧化锰发生了氧化反应
C.电池的正极反应式为MnO2+H2O+e-===MnOOH+OH-
D.当有0.1 mol锌溶解时,流经电解质溶液的电子数为1.204×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
还原沉淀法是处理含铬(含Cr2O72﹣和CrO42﹣)工业废水的常用方法,过程如下:
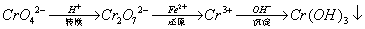
己知转化过程中反应为:2CrO42﹣(aq)+2H+(aq)  Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
Cr2O72﹣(aq)+H2O(1)。转化后所得溶液中铬元素含量为28.6g/L,CrO42﹣有10/11转化为Cr2O72﹣。下列说法不正确的是
A.若用绿矾(FeSO4·7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g
B.溶液颜色保持不变,说明上述可逆反应达到达平衡状态
C.常温下转换反应的平衡常数K=1×1014,则转化后所得溶液的pH=6
D.常温下Ksp[Cr(OH)3]=1×10﹣32,要使处理后废水中c(Cr3+)降至1×10﹣5mol/L,应调溶液的pH=5
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.100mL 2 mol·L-1碳酸钠溶液中,CO32-离子数为0.2NA
B.将10mL 1mol·L-1FeCl3溶液滴入沸水中,所得氢氧化铁胶粒数为0.01NA
C.1 mol Na2O2固体中含离子总数为3NA
D.电解精炼铜时,外电路中转移电子数为2NA个时,阳极铜质量减少64g
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素A、B、C、D的原子序数依次递增.其中A、B、C二种元素基态原子的2p能级上都有未成对电子.且未成对电子个数分别是2、3、2;D与C 可以形成D2C和D2C2两种化合物。回答下列问题:
(1)已知A元素与氢元素形成的某种气态化合物在标准状况下的密度为1.1 6 1 g·L-1,则在该化合物的分子中A原子的杂化方式为 。
(2)A、B、C二种元素的第一电离能由小到大的顺序为 (填元素符号)。
 (3)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子
(3)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子
所需要的能量称为第二电离能I2,依次还有I3、I4、I5……,推测D元素
的电离能第一次突增应出现在第 电离能。
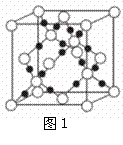
(4)AC2在高温高压下所形成的晶体其晶胞如图1所示。
该晶体的类型属于 晶体.该品体中A原子轨道的
杂化类型为 。
(5)A和C形成原子个数比为1:3的常见离子.推测这种微粒的空间
 构型为 。
构型为 。
(6)C和D形成的一种离子化合物D2C的晶胞结构如图2所示.该晶体
中阳离子的配位数为 。距一个阴离子周围最近的所有阳离子为顶点
构成的几何体为 。已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数为NA.
则晶胞边长a= cm(用含ρ、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是:
A.固体碘转化为紫红色气体,需吸收能量,因共价键被破坏
B.碳酸氢铵是离子化合物,其受热分解产生氨气不仅破坏离子键还破坏了共价键
C.金属和非金属所形成的化学键均为离子键
D.共价键只存在于共价化合物中
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应:
3A(g)+B(g) xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:
n(A)= n(B)=________mol;
B的平均反应速率v(B)=________mol/(L·min);(3)x的值为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的无色溶液,不用其他试剂即可鉴别的是________。
①NaOH、AlCl3 ②NaHCO3、H2SO4 ③Na[Al(OH)4]、NaHSO4 ④Na2CO3、HCl ⑤Na2CO3、NaHCO3、Ca(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com