
| n |
| V |
| 445g |
| 178g/mol |
| 5mol |
| 4.00L |
| 250g��98% |
| 98 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Һ��Al3+ȫ����������ʱ�������������ʵ������ |
| B������Һ��Al3+ȫ����������ʱ����������������� |
| C�������ɳ����������ȫ���ܽ� |
| D�����ij���Ϊ2mol BaSO4��1mol Al��OH��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ڳ�ʪ�����з���������ʴ��������ӦΪFe-3e-�TFe3+ |
| B����ͬ�����£��ִ��ں�ˮ�б��ڵ�ˮ�и�ʴ�� |
| C�����϶�п�ı����������������������������� |
| D��ˮ�����բ�����Դ���������ķ���������ӵ�Դ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ�£�2����������ԭ����ĿΪNA |
| B��4.6������ˮ��Ӧʱʧȥ�ĵ�����ĿΪ0.2NA |
| C���ڱ�״���£�22.4LNH3������������ĿΪNA |
| D��1 L0.5mol?L-1Na2SO4��Һ�������е�Na+������ĿΪ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �������� | NO3- | SO42- | H+ | M |
| Ũ��/��mol?L-1�� | 2 | 1 | 2 | 1 |
| A��Na+ |
| B��Ba2+ |
| C��F- |
| D��S2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������백ˮ��CH3COOH+NH3?H2O=CH3COO-+NH4++H2O |
| B��ͭƬ������������Һ��Cu+Ag+=Cu 2++Ag |
| C��̼��Ƽ�����CO32-+2 CH3COOH=CO2��+2 CH3COO-+H2O |
| D�������ʯ��ˮ�����ᷴӦ��H++OH-=H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
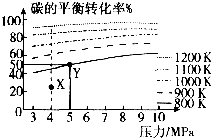 ��֪��ú̿����ɷ�����Ӧ��C��s��+2H2��g��?CH4��g������VL��������Ͷ��amol̼����������ͬʱͨ��2amolH2����������ʹ�䷢��������Ӧ�����̼��ƽ��ת������ѹǿ���¶ȵı仯��ϵ����ͼ��ʾ������˵����ȷ���ǣ�������
��֪��ú̿����ɷ�����Ӧ��C��s��+2H2��g��?CH4��g������VL��������Ͷ��amol̼����������ͬʱͨ��2amolH2����������ʹ�䷢��������Ӧ�����̼��ƽ��ת������ѹǿ���¶ȵı仯��ϵ����ͼ��ʾ������˵����ȷ���ǣ�������| A����������ӦΪ���ȷ�Ӧ | ||
| B����4MPa��1200Kʱ��ͼ��X��v��H2������v��H2���� | ||
C����5MPa��800Kʱ���÷�Ӧ��ƽ�ⳣ��Ϊ
| ||
| D����ҵ��ά��6MPa1000K��������10MPa1000K����Ҫ����Ϊǰ��̼��ת���ʸ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڢ� | B���٢ۢ� |
| C���ڢۢ� | D���٢� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com