
分析 (1)该溶液为无色溶液,有颜色的离子不能存在;
(2)向100mL溶液中加入足量的Ba(NO3)2溶液,得到BaCO3和BaSO4,然后向沉淀中加入足量稀盐酸,BaCO3沉淀溶解,同时得到干燥沉淀BaSO4,说明该溶液中含有CO32、SO42-,则一定不含Ba2+、H+;
(3)(2)过滤后的滤液不含有CO32-、SO42-,能与AgNO3溶液反应生成白色沉淀的只能是Cl-,n(Cl-)=n(AgCl)=$\frac{m}{M}$,c(Cl-)=$\frac{n}{V}$计算.
解答 解:(1)该溶液为无色溶液,而Cu2+为颜色,不能存在无色溶液,
故答案为:Cu2+;
(2)向100mL溶液中加入足量的Ba(NO3)2溶液,得到BaCO3和BaSO4,然后向沉淀中加入足量稀盐酸,BaCO3沉淀溶解,同时得到干燥沉淀BaSO4,说明该溶液中含有CO32-、SO42-,由于CO32-与Ba2+、H+都能发生离子反应,则一定不含Ba2+、H+,
n(CO32-)=n(CO2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,c(CO32-)=$\frac{0.1mol}{0.1L}$=1mol/L,
n(SO42-)=n(BaSO4)=$\frac{23.3g}{233g/mol}$=0.1mol,c(SO42-)=$\frac{0.1mol}{0.1L}$=1mol/L,
故答案为:是;1mol/L;是;1mol/L;Ba2+、H+;
(3)(2)过滤后的滤液不含有CO32-、SO42-,能与AgNO3溶液反应生成白色沉淀的只能是Cl-,n(Cl-)=n(AgCl)=$\frac{14.35g}{143.5g/mol}$=0.1mol,c(Cl-)=$\frac{0.1mol}{0.1L}$=1mol/L,
故答案为:1mol/L.
点评 本题考查了常见离子检验的方法应用,主要是离子共存和反应现象的应用和分析判断,掌握离子性质是解题关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 仅①和④ | B. | 仅①和③ | C. | 仅②和③ | D. | 仅②和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
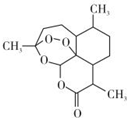 北京时问2015年10月5日,中国女科学家屠哟哟获颁诺贝尔医学奖.屠哟哟从中医古籍里得到启发,用乙醚从青蒿中提取出可以高效抑制疟原虫的成分-青蒿素(结构简式如图),这一发现在全球范围内挽救了数以百万人的生命.下列说法中不正确的是( )
北京时问2015年10月5日,中国女科学家屠哟哟获颁诺贝尔医学奖.屠哟哟从中医古籍里得到启发,用乙醚从青蒿中提取出可以高效抑制疟原虫的成分-青蒿素(结构简式如图),这一发现在全球范围内挽救了数以百万人的生命.下列说法中不正确的是( )| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素能与NaOH溶液反应 | |
| C. | 青蒿素易溶于水、乙醇、苯等溶剂 | |
| D. | 用乙醚从青蒿中提取青蒿素,用到了萃取的原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
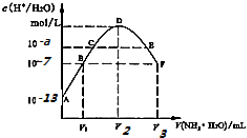
| A. | 稀硫酸的浓度为0.1mol/L | |
| B. | C点溶液pH=14-a | |
| C. | E溶液中存在:c(NH4+)>c(SO42-)>c(H+)>c(OH-) | |
| D. | B到D、D到F所加氨水体积一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
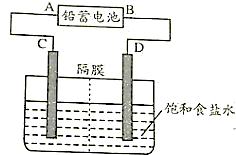
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol•L-1 | B. | 0.4mol•L-1 | C. | 0.2mol•L-1 | D. | 0.6mol•L-1 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上10月月考化学试卷(解析版) 题型:填空题
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。请回答下列问题: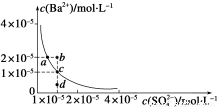
(1)下列说法正确的是__________(填字母序号)。
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
(2)将100 mL 1 mol·L-1 H2SO4加入100 mL含Ba2+ 0.137 g 的溶液中充分反应后,过滤出沉淀,滤液中残留的Ba2+的物质的量浓度为____________(保留三位有效数字)。
(3)将沉淀用100 mL纯水或100 mL 0.01 mol·L-1的H2SO4分别洗涤,两种情况下损失的BaSO4的质量之比为_____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上第一次月考化学卷(解析版) 题型:选择题
下列依据热化学方程式得出的结论正确的是
A.若2H2(g)+O2(g)=2H2O(g)ΔH=—483.6kJ·mol-1,则H2燃烧热为241.8kJ·mol-1
B.若C(石墨,s)=C(金刚石,s)ΔH>0,则石墨比金刚石稳定
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)ΔH=—57.4kJ·mol-1,则20.0gNaOH固体与稀盐酸完全中和 ,放出28
,放出28 .
. 7kJ的热量
7kJ的热量
D.已知2C(s)+2O2(g)=2CO2(g)ΔH1;2C(s)+O2(g)=2CO(g)ΔH2,则ΔH1>ΔH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com