
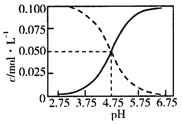
����Ŀ��25��ʱ��c(CH3COOH)+c(CH3COO-)=0.1molL-1�Ĵ��ᡢ�����ƻ����Һ�У�c(CH3COOH)��c(CH3COO-)��pH�Ĺ�ϵ��ͼ��ʾ������������ȷ����( )
A��25��ʱ��CH3COOH�ĵ��볣��K��ֵ5��10-2.75
B����pH����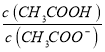 ����
����
C��pH=4����Һ�У�c(CH3COO-)��c(CH3COOH)��c(H+)��c(OH-)
D��pH=5����Һ�У�c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1molL-1
���𰸡�D
��������
����������������ǿ����Һ��c(CH3COOH)��С��c(CH3COO-)�������߱�ʾc(CH3COOH)��ʵ�߱�ʾc(CH3COO-)��A����ͼ��֪��pH=4.75ʱ����Һ��c(H+)=10-4.75mol/L��c(CH3COOH)=c(CH3COO-)=0.05mol/L����CH3COOH�ĵ��볣��K= =c(H+)=10-4.75mol/L����A����B���ɴ������ƽ�ⳣ����֪��
=c(H+)=10-4.75mol/L����A����B���ɴ������ƽ�ⳣ����֪��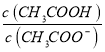 =
=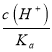 ����pH����c(H+)������
����pH����c(H+)��С����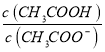 ��С����B����C����ͼ��֪��pH=4ʱ��c(CH3COOH)��c(CH3COO-)����C����D���ɵ���غ��֪��c(Na+)+c(H+)=c(CH3COO-)+c(OH-)������Һ��c(CH3COOH)+c(CH3COO-)=0.1molL-1�������ɵ�c(Na+)+c(H+)+c(CH3COOH)-c(OH-)=0.1molL-1����D��ȷ����ѡD��
��С����B����C����ͼ��֪��pH=4ʱ��c(CH3COOH)��c(CH3COO-)����C����D���ɵ���غ��֪��c(Na+)+c(H+)=c(CH3COO-)+c(OH-)������Һ��c(CH3COOH)+c(CH3COO-)=0.1molL-1�������ɵ�c(Na+)+c(H+)+c(CH3COOH)-c(OH-)=0.1molL-1����D��ȷ����ѡD��


 ��ĩ�óɼ�ϵ�д�
��ĩ�óɼ�ϵ�д� 99��1������ĩ��ѵ��ϵ�д�
99��1������ĩ��ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ���ǻ�ѧʵ���ҵij���װ�ã����ж�����;�����¸�����;�Ͳ�������ȷ����
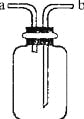
����֪��2H2S+SO2��3S+2H2O��
A.����CO2��ƿ�ڷ�һ�����Ũ���ᣬ��a����
B.�����ռ�O2��ƿ�ڳ���ˮ����b����
C.�ṩ����CO��ƿ�ڳ���CO��b�ӽ�ˮ��
D.����H2S��SO2��Ӧ��װ�ã���aͨ��H2S��bͨ��SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�Ҹոշ�����ij��Ԫ�ص�ԭ�ӣ���������ag��һ��12C��ԭ��������bg��NA�ǰ����ӵ�������ֵ������˵������ȷ���ǣ� ��
A.��ԭ�ӵ�Ħ��������aNAg/mol
B.Wg��ԭ�ӵ����ʵ�����![]() mol
mol
C.��ԭ�ӵ����ԭ������Ϊ![]()
D.����֪��Ϣ�ɵ�NA=![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��H2(g)��![]() O2(g)=H2O(g) ��H1
O2(g)=H2O(g) ��H1
![]() N2(g)��O2(g)=NO2(g) ��H2
N2(g)��O2(g)=NO2(g) ��H2
![]() N2(g)��3/2H2(g)=NH3(g) ��H3
N2(g)��3/2H2(g)=NH3(g) ��H3
��Ӧ2NH3(g)��![]() O2(g)=2NO2(g)��3H2O(g)����HΪ�� ��
O2(g)=2NO2(g)��3H2O(g)����H�� ��
A. 2��H1��2��H2��2��H3B. ��H1����H2����H3
C. 3��H1��2��H2��2��H3D. 3��H1��2��H2��2��H3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�ݻ�һ�����ܱ������У������еĿ��淴Ӧ��A��g����B��g��![]() xC��g��������Ӧ���ȣ���ͼ����ʾ�ķ�Ӧ���ߣ����ж϶�ͼ����˵������ȷ���ǣ�T��ʾ�¶ȣ�P��ʾѹǿ��C%��ʾC�����������
xC��g��������Ӧ���ȣ���ͼ����ʾ�ķ�Ӧ���ߣ����ж϶�ͼ����˵������ȷ���ǣ�T��ʾ�¶ȣ�P��ʾѹǿ��C%��ʾC�����������

A. P3��P4��y���ʾB��ת���� B. P3��P4��y���ʾB���������
C. P3��P4��y���ʾ���������ܶ� D. P3��P4��y���ʾ���������ܶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I����Ȼ���е����ʾ�������Ի�������ʽ���ڣ�Ϊ�˱����о������ã�����Ի������з�����ᴿ������A��B��C��D����ѧ�����Ļ���������ᴿ��װ�á�
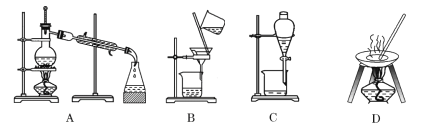
����ݻ���������ᴿ��ԭ�����ش�������ʵ������Ҫʹ������װ�á���A��B��C��D �����ʵ��Ŀո��С�
(1)̼�������Һ�з����̼���__________��
(2)�Ȼ�����Һ�з�����Ȼ���___________��
(3)����39�����Ҵ���Һ___________��
(4)��������Ȼ�����Һ____________��
��.��������ѧ������ʵ���е�Ӧ���������֪ʶ�������
��֪ij�����Ȼ�����Һ���ΪVmL����Һ�ܶ�Ϊd g/cm3����������Ϊw�����ʵ���Ũ��Ϊc mol/L����Һ�к�NaCl������Ϊm g��
(1)��m��V��ʾ��Һ�����ʵ���Ũ����_________
(2)��w��d��ʾ��Һ�����ʵ���Ũ����_________
(3)��c��d��ʾ��Һ������������__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����������ͨ��30 mLŨ��Ϊ10.00 mol/L����������Ũ��Һ�У���������ʱ�����Һ���γ�NaCl��NaClO��NaClO3������ϵ�������ж���ȷ����( )
A.��NaOH��Ӧ������Ϊ0.25 mol
B.n(Na+)��n(Cl-) ����Ϊ7��3
C.����Ӧ��ת�Ƶĵ���Ϊn mol����0.15n0.25
D.n(NaCl):n(NaClO):n(NaClO3)����Ϊ11��2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɺͽṹ���� ��ʾ���л��ﹲ��(����������ṹ)(����)
��ʾ���л��ﹲ��(����������ṹ)(����)
A. 24��B. 28��C. 32��D. 36��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ��XΪ��Դ��YΪ������ʳ��ˮ�ͷ�̪��Һ����ֽ����ֽ�������һ��KMnO4��Һ��ͨ���Y������Ϻ�ɫ����d����ɢ�������ж���ȷ���ǣ� ��
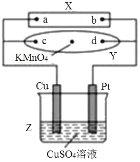
A.��ֽ��c�㸽������ɫ
B.Cu�缫������С��Pt�缫��������
C.Z����Һ��pH�ȼ�С��������
D.��Һ�е�SO42-��Cu�缫�����ƶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com