
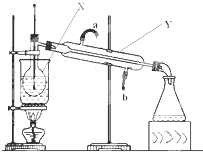
 用NaOH固体配制100mL2.0mol/L NaOH溶液,其操作可以分为以下几步(容量瓶已检查完好,瓶口处不漏水):
用NaOH固体配制100mL2.0mol/L NaOH溶液,其操作可以分为以下几步(容量瓶已检查完好,瓶口处不漏水):| n |
| V |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
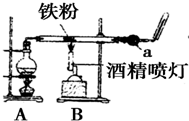 如图是铁与水蒸气反应的实验装置.某同学在硬质玻璃管中放入足量还原性铁粉和少量石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,进行高温下铁与水蒸气反应的实验.请回答下列问题:
如图是铁与水蒸气反应的实验装置.某同学在硬质玻璃管中放入足量还原性铁粉和少量石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,进行高温下铁与水蒸气反应的实验.请回答下列问题:| 操作 | 现象 | 结论 | 解释(用离子方 程式表示) |
| 将反应后的固体全部取出置于烧杯中,加入足量的盐酸,溶解后过滤,立即向滤液中滴加KSCN溶液,观察溶液的颜色. | 滴加KSCN溶液后,溶液不变红色 | ① ② |
查看答案和解析>>
科目:高中化学 来源: 题型:
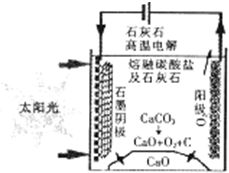 按要求回答:
按要求回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、棉花、木材及草类的纤维都属于天然纤维 |
| B、所有分散系的分散质粒子都能透过半透膜 |
| C、16O与18O互为同素异形体 |
| D、H2、D2、T2互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上层为紫色液体,下层为无色液体 |
| B、均为紫色液体 |
| C、上层为无色液体,下层为紫色液体 |
| D、均为无色液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com