
 下图中X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.
下图中X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.分析 X为直流电源,Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒,接通电路后发现d附近显红色,则d附近生成氢氧根离子,则d极为电解池阴极,d电极上氢离子放电生成氢气和氢氧根离子,c为阳极,c电极上氯离子放电,则a是直流电源正极,b是直流电源负极;电子从原电池的负极流向电解池的阴极,再到阳极,最后流入原电池的正极;结合电解池中两极上的反应分析,(3)中根据电子守恒和电解池的总反应计算.
解答 解:(1)①由以上分析可知b为负极,故答案为:负;
②Z槽中e与原电池正极相连为阳极;故答案为:阳;
(2)d附近显红色说明有碱生成,所以d为电解池的阴极,由此推知c为阳极,e 为阳极,f 为阴极,a为正极,b负极,
①c为阳极,氯离子放电,电极反应式为:2Cl--2e-=Cl2↑,故答案为:2Cl--2e-=Cl2↑;
②电解氯化钠溶液的化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2NaOH,故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2NaOH;
③e 为阳极,铜是活性电极,所以电极上铜放电,电极反应式为:Cu-2e-=Cu2+,故答案为:Cu-2e-=Cu2+;
(3)设电路中转移的电子为xmol,根据e极:Cu-2e-=Cu2+,△m=64 得e极质量减轻:32x(g);
f极:Cu2++2e-=Cu,△m=64 得f极质量增重:32x(g),所以有:32x+32x=1.28,得x=0.02mol,
故答案为:0.02.
点评 本题主要考查了电解池的电极反应及电极中的有关计算,难度不大,解题时注意在Z中铜是活性电极.


科目:高中化学 来源: 题型:解答题
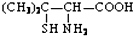 ,请写出青霉氨基酸可能具有的一种化学性质能与碱发生中和反应.
,请写出青霉氨基酸可能具有的一种化学性质能与碱发生中和反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 吸热反应在一定条件下也能发生 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g);△H=-235.8 kJ/mol 则氢气的燃烧热为235.8KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
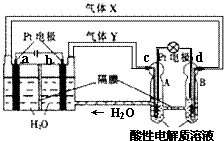 “天宫一号”RFC供电系统是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
“天宫一号”RFC供电系统是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )| A. | 当转移0.1 mol电子,a极产生2.24 L H2 | |
| B. | b电极反应是:4H2O+4e-═2H2↑+4OH- | |
| C. | d电极反应是:O2+4H++4e-═2H2O | |
| D. | c极上发生还原反应,B中H+经隔膜进入A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.6 g C7H8和C3H8O3的混合物中所含氢原子总数为0.4NA | |
| B. | 标准状况下,11.2 L C2H5OH中所含的分子数为0.5NA | |
| C. | 常温常压下,0.1 mol Na2O2与CO2反应转移的电子数目为0.4NA | |
| D. | 在1 L 0.1 mol•L-1碳酸钠溶液中,阴离子总数等于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含溶质质量相等 | B. | 所含溶质物质的量氨水多 | ||
| C. | 溶液物质的量浓度相等 | D. | 电离度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com