
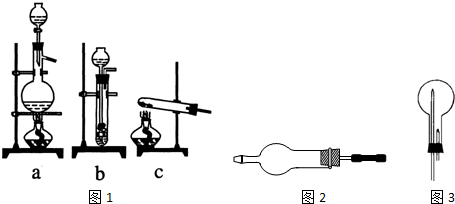
���� ��1��ʵ�������Ȼ�������������ڼ����������Ʊ����������ݷ�Ӧ��״̬�ͷ�Ӧ����ѡ����װ�ã�
��2��һˮ�ϰ����ȷֽ����ɰ�����ˮ��
��3������Ϊ�������壬Ӧѡ����Ը�����������ͼ��������״˵�������ƣ�
��4�����ݰ����ܶ�С�ڿ����ܶȣ�����Ϊ������������ʽ��
��5��������ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ���������笠����Ӻ����������ӣ���Һ�Լ��ԣ�
��6����NH3 9L ����� 1L������M=$\frac{m}{n}$����ƽ����Է���������
��� �⣺��1���Ȼ�������������ڼ����������ɰ������Ȼ��ƺ�ˮ������ʽ��2NH4Cl+Ca��OH��$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O����Ӧ��Ϊ������Һ�壬��Ӧ����Ϊ���ȣ�����Ӧѡ��a��
�ʴ�Ϊ��2NH4Cl+Ca��OH��2 $\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��a��
��2��ʵ������ȡ�����������ü���Ũ��ˮ�ķ���������ʽ��NH3•H2O$\frac{\underline{\;��\;}}{\;}$NH3��+H2O���ʴ�Ϊ��NH3•H2O$\frac{\underline{\;��\;}}{\;}$NH3��+H2O��
��3������Ϊ�������壬Ӧѡ����Ը��������ʯ��Ϊ���Ը�������Ը��ﰱ����ͼ������Ϊ����ܣ�����ʱӦ��ڽ��룬���Ը���ʱ�������ķ������Ҷˣ�
�ʴ�Ϊ������ܣ���ʯ�ң��Ҷˣ�
��4�������ܶ�С�ڿ����ܶȣ�Ӧѡ�������������ռ�������Ӧ�̽�����������Ϊ�������壬�ܹ�ʹ��ɫʯ����ֽ�����������ú�ɫʯ����ֽ���飻
�ʴ�Ϊ���̣�ʪ���ɫʯ���ֽ������
��5��������ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ���������笠����Ӻ����������ӣ���Һ�Լ��ԣ�����ʽ��NH3+H2O?NH3•H2O?NH4++OH-��
�ʴ�Ϊ��NH3+H2O?NH3•H2O?NH4++OH-��
��6����NH3 9L ����� 1L�����ݰ���٤���������ɿ�֪���������ʵ���֮��Ϊ9��1����ƽ����Է�������=$\frac{19��9+29��1}{10}$=18.2��
�ʴ�Ϊ��18.2��
���� ���⿼���������ʵ�����Ʊ�����ȷ����ʵ�����Ʊ�ԭ���������������ǽ���ؼ�����Ŀ�ѶȲ���


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��3-����ϩ�ķ���ʽ��C4H6 | B�� | ������ĵ���ʽ��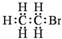 | ||
| C�� | ��ȩ�Ľṹʽ��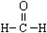 | D�� | �����ǵĽṹ��ʽ��CH2OH��CHOH��4CHO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
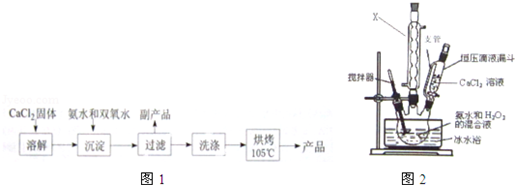
| ʵ����� | ��1�� | ��2�� | ��3�� | ��4�� |
| ����KMnO4���/mL | 19.98 | 20.02 | 20.20 | 20.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
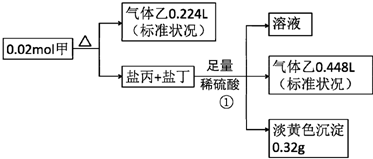
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱ��������������Ӧ | B�� | �ϳɰ���Ӧ | ||
| C�� | �ð����ϳ����� | D�� | ����þ�ڵ�����ȼ������Mg3N2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
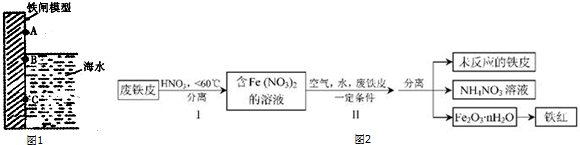
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
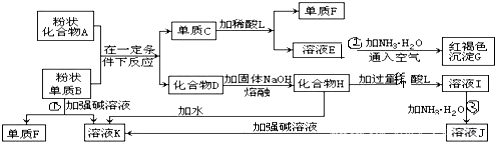
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ӳɡ����������� | B�� | �ӳɡ��ӳɡ��Ӿ� | C�� | �ӳɡ���ȥ���Ӿ� | D�� | �ӳɡ�ȡ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com