氮有多种氧化物,其中N
2O
5是一种新型硝化剂,其性质和制备收到人们的关注.
(1)一定温度下,在恒容密闭容器中N
2O
5可发生下列反应:
2N
2O
5(g)?4NO
2(g)+O
2(g);△H>0
①反应达到平衡后,若再通入一定量氩气,则N
2O
5的转化率将______(填“增大”、“减小”、“不变”).
②如表为反应在T
1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol?L-1 | 5.00 | 3.52 | 2.48 |
则500s内N
2O
5的分解速率为______.
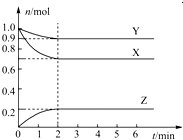
③一定温度下,在2L恒容密闭容器中加入2molN
2O
5,达到平衡时,气体的压强为原来的
,(不考虑NO
2聚合成N
2O
4),则N
2O
5的转化率a
1=______,该温度下反应的平衡常数K=______.
(2)如图1所示装置可用于制备N
2O
5,则N
2O
5在电解池的______区生成,其电极反应式为______.
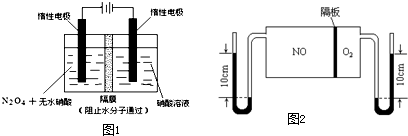
(3)如图2:V(NO):V(O
2)=3:1.当抽去NO和O
2之间的隔板后,NO和O
2反应后成NO
2,部分NO
2聚合成N
2O
4(N
2O
4此时为气态).当体系达到平衡后,U形毛细管两端汞面高度差由反应前10cm变为7.1cm.假设温度不变,且隔板及U形毛细管的体积都忽略不计,此时混合气体的平均相对分子质量为______.




 高中必刷题系列答案
高中必刷题系列答案