
| A. | ⅠA元素的电负性从上到下逐渐减小,ⅦA元素的第一电离能从上到下逐渐减小 | |
| B. | 电负性的大小可以作为衡量元素的金属性和非金属性强弱的尺度 | |
| C. | NaH的存在能支持可将氢元素放在ⅦA的观点 | |
| D. | 氢原子中只有一个电子,故氢原子只有一个原子轨道 |
分析 A.同一主族元素原子的第一电离能I1变化规律是从上到下逐渐减小;非金属性越强,电负性越大,金属性越强,电负性越小;
B.金属的电负性一般小于1.8,非金属的电负性一般大于1.8;
C.NaH中的H元素最低为-1,ⅦA族中元素的最低化合价为-1价;
D.氢原子中只有一个电子,但不是只有一个轨道.
解答 解:A.ⅠA元素的电负性从上到下,非金属性减弱,金属性增强,所以电负性从上到下逐渐减小,Ⅶ元素的第一电离能从上到下逐渐减小,故A正确;
B.金属的电负性一般小于1.8,非金属的电负性一般大于1.8,所以电负性的大小可以作为衡量元素的金属性和非金属性强弱的尺度,故B正确;
C.NaH中的H元素最低为-1,可以放在放在ⅦA族中,故C正确;
D.氢原子中有一个电子,但轨道是人们规定的,只是空轨道而已,氢原子不只有一个轨道,故D错误;
故选D.
点评 本题考查元素电离能、电负性变化规律,明确电离能与失电子难易程度、电负性与得电子强弱关系是解本题关键,侧重考查运用知识解答问题能力,熟练掌握元素周期律知识,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 实验编号 | 待测NaOH溶液的体积/mL | 滴定完成时,消耗盐酸的体积/mL |
| 1 | 20.00 | 22.40 |
| 2 | 20.00 | 22.42 |
| 3 | 20.00 | 22.38 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
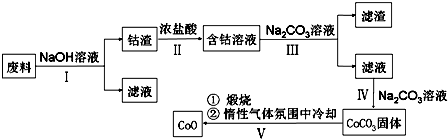
| A. | 第Ⅰ步反应后得到的滤液主要是含铝溶液 | |
| B. | 第Ⅱ步中盐酸表现出酸性、还原性,且必须过量 | |
| C. | 第Ⅲ步中Na2CO3主要作用是使Fe3+沉淀,滤渣主要为Fe(OH)3 | |
| D. | 第Ⅳ步操作为过滤,第Ⅴ步煅烧后,也可以在一氧化碳气体氛围中冷却 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子晶体中,只存在离子键,不可能存在其他化学键 | |
| B. | 原子晶体中,只存在共价键;稀有气体的原子能形成分子晶体 | |
| C. | NaHSO4、NaOH晶体中的阴、阳离子个数比均为1:2 | |
| D. | 晶体熔点:金刚石>食盐>干冰>冰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入Al能放出H2的溶液中:NH4+,SO42-,Br-,NO3- | |
| B. | 通入过量SO2气体的溶液中:Fe3+、NO3-、Ba2+、H+ | |
| C. | 无色强酸性溶液中:Na+、Cl-、SO42-、Cu2+ | |
| D. | c(I-)=0.1 mol•L-1的溶液中:Na+、Fe2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
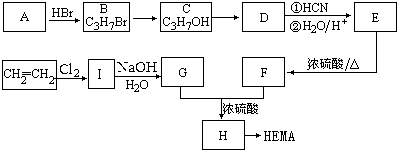
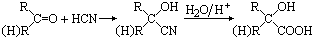
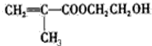 甲基丙烯酸羟乙酯
甲基丙烯酸羟乙酯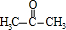 +2H2O.
+2H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
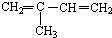 与Br2按物质的量之比1:1发生1,4加成反应的化学方程式CH2=C(CH3)CH=CH2+Br2→CH2BrC(CH3)=CHCH2Br.
与Br2按物质的量之比1:1发生1,4加成反应的化学方程式CH2=C(CH3)CH=CH2+Br2→CH2BrC(CH3)=CHCH2Br. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com