
 Ti��Fe��Cr��Mn�Ⱦ�Ϊ����Ԫ�أ����������������Ų����������Ҫ���ã����䵥�ʺͻ������Ӧ���о���Ŀǰ��ѧ�о���ǰ��֮һ����ش��������⣺
Ti��Fe��Cr��Mn�Ⱦ�Ϊ����Ԫ�أ����������������Ų����������Ҫ���ã����䵥�ʺͻ������Ӧ���о���Ŀǰ��ѧ�о���ǰ��֮һ����ش��������⣺���� ��1�������������ԭ�������ع���������д������ϵĵ��Ӵ���ȫ����������ȫ��ʱ���ȶ������Ӳ�����ʧȥ��
��2��Cuλ�����ڱ��������ڢ�B�壬Ϊds��Ԫ�أ���ʢ������ͭˮ��Һ���Թ�����백ˮ�������γ�������ͭ�����������Ӱ�ˮ��������ͭ�ܽ�õ��İ���ͭ�����ӣ���Һ������ɫ����Һ�������뼫�Խ�С���ܼ��Ҵ������ɵ�[Cu��NH3��4]SO4�����õ�����ɫ�ľ��壻
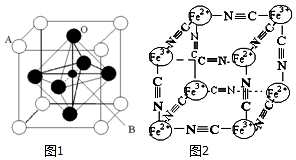
��3�����ݾ�̯�����㾧����A��B��Oԭ����Ŀ������ȷ����ѧʽ��
��4������ͼ2�����ṹ��֪�������к���Fe2+�ĸ���Ϊ4��$\frac{1}{8}$=$\frac{1}{2}$��Fe3+�ĸ���Ϊ4��$\frac{1}{8}$=$\frac{1}{2}$��CN-�ĸ���Ϊ12��$\frac{1}{4}$=3������Fe2+��Fe3+��CN-�ĸ�����Ϊ1��1��6�����ݻ��ϼ۴�����Ϊ���֪��x=1������Ļ�ѧʽ�ɱ�ʾΪKFe2��CN��6��
��� �⣺��1�������������ԭ�������ع�����������֪CrԪ�ػ�̬ԭ�ӵ����Ų�ʽΪ1s22s22p63s23p63d54s1����Ԫ�ص�3d�ܼ���4s�ܼ��ϵĵ��Ӷ��Ǽ۵��ӣ�MnԪ�ػ�̬ԭ�ӵļ۵����Ų�ʽΪ3d54s2����Mn2+ת��ΪMn3+ʱ��3d�ܼ��ɽ��ȶ���3d5�����״̬ת��Ϊ���ȶ���3d4״̬��Ҫ�������϶ࣻ��Fe2+ת��ΪFe3+ʱ��3d�ܼ��ɲ��ȶ���3d6ת��Ϊ�ȶ���3d5��������ȶ�״̬����Ҫ���������Ҫ�٣�
�ʴ�Ϊ��1s22s22p63s23p63d54s1���ѣ�
��2��Cuλ�����ڱ��������ڢ�B�壬Ϊds��Ԫ�أ�������ͭ�백ˮ������Ӧ��Cu��OH��2+4NH3•H2O=[Cu��NH3��4]2++2OH-+4H2O�������ܽ⣬�����Һ�м��Ҵ������ɵ�[Cu��NH3��4]SO4�ڼ��Լ��Ե��Ҵ����ܽ�ȼ�С�������õ�����ɫ�ľ��壬������[Cu��NH3��4]2+�У�Cu�γ�4���Ҽ���d������Ӳ����ӻ�������sp3�ӻ���Ϊƽ���ı��νṹ��
�ʴ�Ϊ��ds��Cu��OH��2+4NH3•H2O=[Cu��NH3��4]2++2OH-+4H2O��������ƽ���ı��Σ�
��3��������Aԭ����Ŀ=8��$\frac{1}{8}$=1��Bԭ����Ŀ=1��Oԭ����Ŀ=6��$\frac{1}{2}$=3���������⾧��Ļ�ѧʽΪ��ABO3��
�ʴ�Ϊ��ABO3��
��4������ͼ2�����ṹ��֪�������к���Fe2+�ĸ���Ϊ4��$\frac{1}{8}$=$\frac{1}{2}$��Fe3+�ĸ���Ϊ4��$\frac{1}{8}$=$\frac{1}{2}$��CN-�ĸ���Ϊ12��$\frac{1}{4}$=3������Fe2+��Fe3+��CN-�ĸ�����Ϊ1��1��6�����ݻ��ϼ۴�����Ϊ���֪��x=1������Ļ�ѧʽ�ɱ�ʾΪKFe2��CN��6��
�ʴ�Ϊ��KFe2��CN��6��
���� ���⿼���Ϊ�ۺϣ������ʽṹ�Ŀ��飬Ϊ�߿��������ͺ�Ƶ���㣬���ؿ���ѧ���ķ��������ͼ�����������Ŀ�漰��������Ų��������ܡ���λ������������ȣ�ּ�ڿ���ѧ���Ի���֪ʶ�����ռ��ۺ�Ӧ�ã��Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
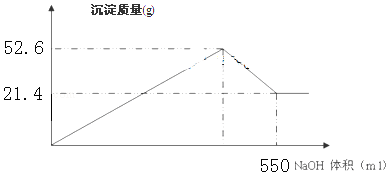
| A�� | ����̿��SO2��Na2O2����ʹƷ����Һ��ɫ����ԭ����ͬ | |
| B�� | �ǽ��������ﲻһ���������������������������Ǽ��������� | |
| C�� | ͬ��ͬѹ�£�������ͬ���������ۣ��ֱ���������ϡ�����ϡ���ᷴӦ����������������ͬ | |
| D�� | ��SO2����ͨ��BaCl2��Һ��������δ���������ɣ�����ͨ��NO2���г������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
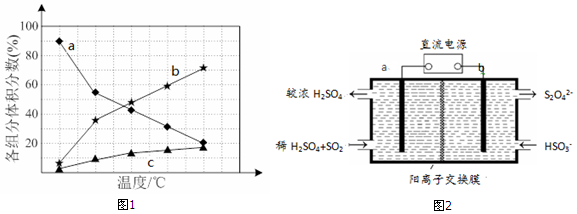
| A�� | ������ʹ���Ը��������Һ��ɫ | B�� | ������ʹ���Ը��������Һ��ɫ | ||
| C�� | ��ʹ�����Ļ�����ǿ | D�� | ����ʹ���Ļ�����ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4 �� | B�� | 6 �� | C�� | 8 �� | D�� | 10 �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4��SiH4��GeH4��SnH4 | B�� | NH3��PH3��AsH3��SbH3 | ||
| C�� | H2O��H2S��H2Se��H2Te | D�� | HCl��HBr��HI��HF |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
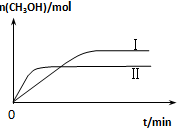 �о�CO2�����öԴٽ���̼���Ĺ���������Ҫ�����壮
�о�CO2�����öԴٽ���̼���Ĺ���������Ҫ�����壮| �� �� | �� | �� |
| ��Ӧ��Ͷ���� | 1molCO2��3molH2 | a molCO2��b molH2��c molCH3OH��g����c molH2O��g�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com