
下表是元素周期表的短周期部分,表中字母分别表示一种元素,回答下列问题:
| a | | | |||||
| | | | c | e | f | g | |
| | | b | d | | | h | |
(1)NH3<H2O<HF(2) 离子键、共价键 离子
离子键、共价键 离子
(3)CH2=CH2 加聚反应 加成反应
CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O 取代反应(酯化反应或可逆反应)
CH3COOCH2CH3+H2O 取代反应(酯化反应或可逆反应)
2CH2CH2OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
解析试题分析:根据元素在周期表中的相对位置可知,a~h元素分别是H、Al、C、Si、N、O、F、Cl。
(1)同周期自左向右非金属性逐渐增强,同主族自上而下非金属性逐渐减弱。非金属性越强,氢化物的稳定性越强,则e、f、g三种元素气态氢化物的稳定性由弱到强的顺序为NH3<H2O<HF。
(2)氮元素的氢化物是氨气,含有极性键的共价化合物,电子式是 。氨气和硝酸反应生成硝酸铵,该化合物属于离子化合物,含有离子键和极性键。
。氨气和硝酸反应生成硝酸铵,该化合物属于离子化合物,含有离子键和极性键。
(3)乙烯的产量是衡量一个国家石油化工发展水平的标志,即A是乙烯。乙烯含有碳碳双键,则A的结构简式为CH2=CH2 。乙烯发生加聚反应生成聚乙烯。乙烯能和水发生加成反应生成乙醇。乙醇和乙酸发生酯化反应生成乙酸乙酯,反应的化学方程式是CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O。乙醇在催化剂的作用下发生氧化反应生成乙醛,反应的化学方程式是2CH2CH2OH+O2
CH3COOCH2CH3+H2O。乙醇在催化剂的作用下发生氧化反应生成乙醛,反应的化学方程式是2CH2CH2OH+O2 2CH3CHO+2H2O。
2CH3CHO+2H2O。
考点:考查元素周期表的结构以及元素周期律的应用、常见化学用语的书写
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。


科目:高中化学 来源: 题型:
| a | |||||||
| b | c | d | |||||
| e | f | g | |||||
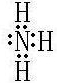
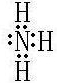
查看答案和解析>>
科目:高中化学 来源: 题型:
| a | |||||||
| b | c | d | |||||
| e | f | g | |||||

| ||
| △ |
| ||
| △ |
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高一下学期期末考试化学试卷(解析版) 题型:填空题
下表是元素周期表的短周期部分,表中字母分别表示一种元素,回答下列问题:
|
a |
|
|
|||||
|
|
|
|
c |
e |
f |
g |
|
|
|
|
b |
d |
|
|
h |
|
(1)e、f、g三种元素气态氢化物的稳定性由弱到强的顺序为(用化学式表示)__________。
(2)元素e的气态氢化物电子式为__________,该氢化物与其最高价氧化物的水化物反应生成的物质所含化学键类型为___________,属于_______化合物(填离子或共价)。
(3)a、c两种元素可形成多种化合物,其中化合物A的产量是衡量一个国家石油化工发展水平的标志,则: A的结构简式为____________;以A为原料,可制得当今世界上产量最大的塑料产品,该反应类型为_________________;A可与H2O反应生成化合物B,该反应类型为__________________。B与CH3COOH反应生成有果香气味的产物,该反应的化学方程式为_____________________________________________________ ;该反应类型为_____________。B在以铜为催化剂时反应生成有刺激性气味的产物,该反应的化学方程式为_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014届山东省高一下学期期中考试化学试卷(解析版) 题型:填空题
(14分)下表是元素周期表的短周期部分,表中字母分别表示一种元素。请回答下列问题:
|
a |
|
|
|||||
|
|
|
|
b |
c |
d |
|
|
|
e |
|
f |
|
|
g |
|
|
(1) f元素在周期表中的位置是第 周期第 族。
(2) e 与f两元素最高价氧化物的水化物相互反应的化学方程式为
_________________________________________________
(3)e在空气中燃烧的产物所含化学键的类型为__________、__________。
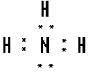
(4) 化合物ca3的电子式为 ,c和d两种元素氢化物的稳定性更强的是 _______(填物质的化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com